RNA修饰项目 | 靶向NAT10,ac4C修饰稳定ETS2与KRT8 mRNA促进胰腺癌进展
胰腺癌(pancreatic cancer, PC)是当前预后最差的恶性肿瘤之一,五年生存率仅约13%。尽管手术、放化疗及靶向治疗不断进展,但总体疗效提升有限。免疫检查点抑制剂,尤其是PD-1/PD-L1通路阻断,在多种实体瘤中已取得显著疗效,但在胰腺癌中效果不佳,主要原因在于其典型的“冷肿瘤”特征和高度免疫抑制性的肿瘤微环境。
近年来,RNA表观修饰在肿瘤发生发展中的作用逐渐受到关注。ac4C(N4-乙酰胞苷)是一种进化保守的RNA修饰形式,其“写入酶”NAT10已被证实在多种肿瘤中异常高表达,并参与RNA稳定性调控和恶性进展。然而,在胰腺癌中,NAT10是否通过ac4C修饰同时调控肿瘤细胞内在恶性行为与免疫逃逸过程?其是否可作为突破免疫治疗耐药的干预靶点?

2025年11月7日,江南大学附属医院及无锡医学院团队在《Cell Death & Disease》上发表了题为“Targeting the ac4C ‘Writer’ NAT10 enhances pancreatic cancer immunotherapy via dual modulation of CD8⁺ T cells and tumor cells”的重要研究。研究发现,NAT10在胰腺癌组织中显著高表达,并与不良预后相关。机制上,NAT10通过ac4C修饰增强ETS2与KRT8 mRNA稳定性:一方面通过ETS2形成NAT10-ETS2-PD-L1正反馈环路,抑制CD8⁺ T细胞浸润;另一方面通过稳定KRT8促进肿瘤细胞增殖与转移。动物实验表明,NAT10抑制联合PD-L1抗体治疗显著增强抗肿瘤免疫效果,提示其为潜在联合治疗靶点。
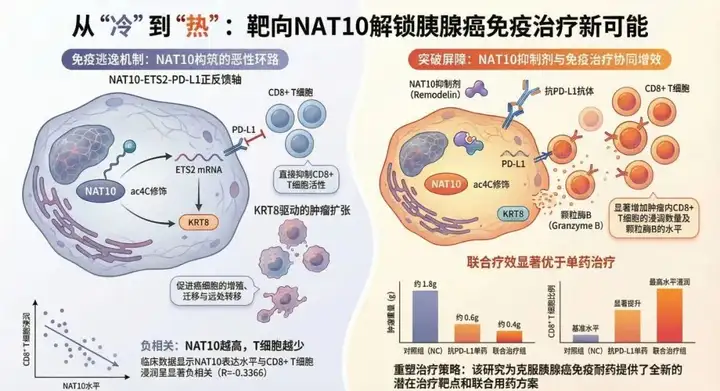
注:ai生成
研究技术路线
关键研究结果
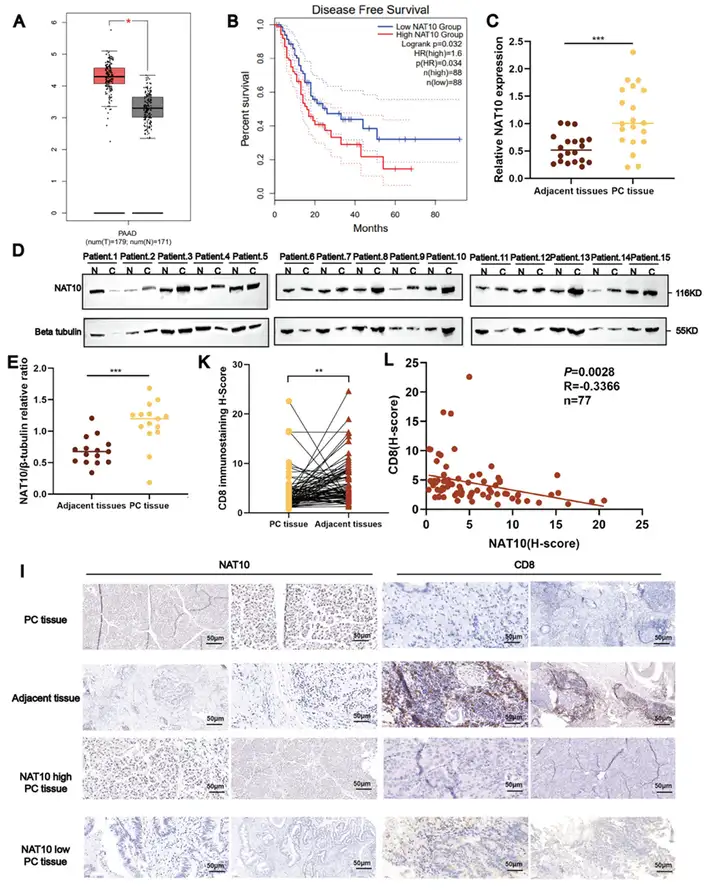
1.NAT10在胰腺癌中高表达并与不良预后及免疫抑制相关
数据库分析与临床样本验证一致表明,NAT10在胰腺癌组织中显著高表达,并与较差的疾病无进展生存期密切相关。同时,IHC结果显示NAT10高表达区域CD8⁺ T细胞浸润显著减少,且二者呈负相关关系。这提示NAT10不仅参与肿瘤进展,还可能通过抑制免疫细胞浸润参与免疫逃逸。
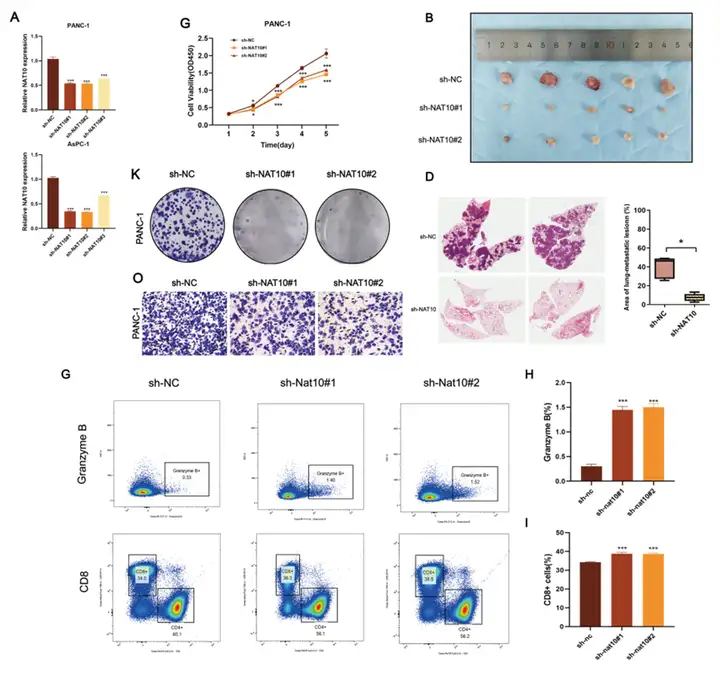
2.NAT10在体内外促进胰腺癌恶性进展
功能实验显示,NAT10敲低显著抑制细胞增殖、克隆形成及迁移侵袭能力,而过表达增强恶性表型。体内模型进一步证实,NAT10敲低显著降低皮下成瘤重量并减少肺转移灶。同时在免疫完整小鼠中,NAT10敲低增强CD8⁺ T细胞浸润与Granzyme B表达,说明其同时促进肿瘤生长与免疫抑制。
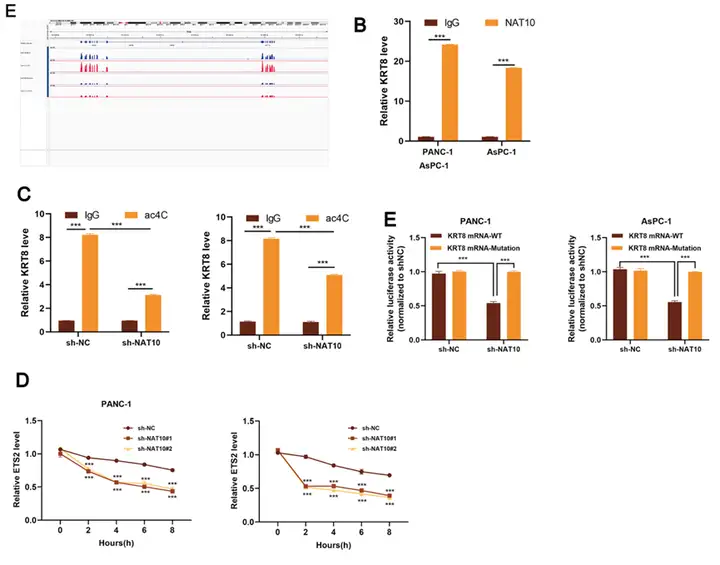
3. 翻译抑制依赖于序列特异性碱基配对与环状拓扑结构
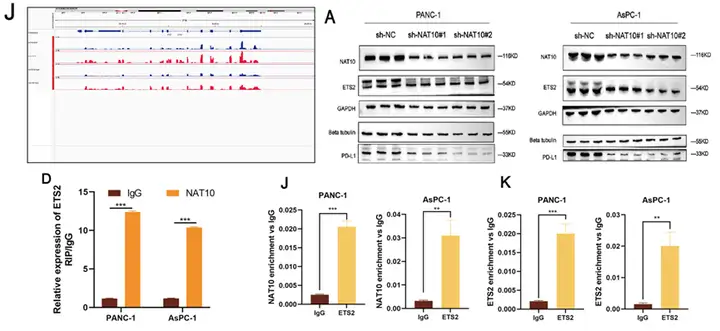
多组学分析显示KRT8 mRNA存在ac4C修饰位点。RIP与acRIP实验(由表观生物提供)证实NAT10直接结合并乙酰化KRT8 mRNA。mRNA稳定性实验显示NAT10敲低显著降低KRT8半衰期,双荧光素酶实验证实调控依赖ac4C位点。说明NAT10通过稳定KRT8增强肿瘤增殖与迁移能力。
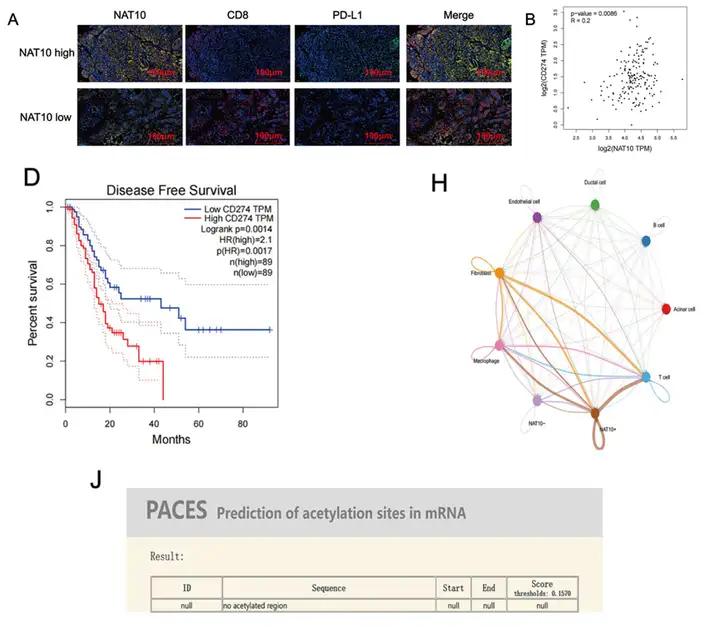
4.NAT10间接调控PD-L1并增强肿瘤-免疫细胞相互作用
mIHC与数据库分析显示NAT10与PD-L1表达呈正相关,且PD-L1高表达与不良预后相关。单细胞分析显示高NAT10上皮细胞与T细胞间通讯增强。acRIP-seq未发现PD-L1直接ac4C位点,提示其通过间接机制调控PD-L1表达并增强免疫抑制信号。
5.NAT10通过稳定ETS2形成NAT10–ETS2–PD-L1正反馈轴
整合RNA-seq、acRIP-seq与ATAC-seq(由表观生物提供)筛选出ETS2为关键调控因子。acRIP-seq显示ETS2存在ac4C位点,RIP-qPCR证实NAT10直接结合ETS2 mRNA并增强其稳定性。ChIP-qPCR显示ETS2可结合NAT10与PD-L1启动子,形成正反馈环路,持续增强PD-L1表达与免疫抑制。
6.NAT10抑制联合PD-L1阻断显著增强抗肿瘤疗效
在联合治疗模型中,NAT10抑制剂与抗PD-L1抗体联用显著降低肿瘤重量,疗效优于单药治疗。流式细胞术显示联合治疗显著提高CD8⁺ T细胞比例及Granzyme B表达,提示联合干预可协同增强抗肿瘤免疫反应。
结论与讨论
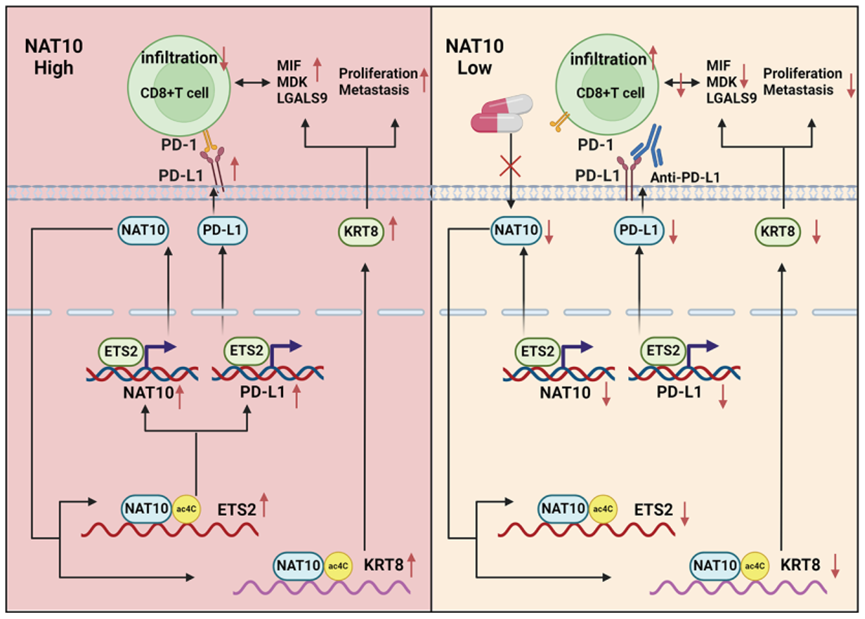
该研究从RNA表观修饰层面系统解析了胰腺癌免疫逃逸的分子基础,揭示NAT10作为ac4C“写入酶”在肿瘤进展与免疫调控中的枢纽作用。不同于既往仅关注其促增殖功能,作者提出NAT10通过稳定ETS2与KRT8 mRNA,分别驱动PD-L1依赖的免疫抑制和肿瘤细胞恶性表型,形成连接RNA修饰、转录调控与免疫检查点通路的正反馈网络。同时,研究指出NAT10可能还存在ac4C非依赖性调控方式,其在不同免疫细胞亚群中的功能仍有待进一步厘清。在转化层面,虽然NAT10抑制剂联合PD-L1阻断显示出协同潜力,但其特异性、安全性与药代动力学特征仍需优化。整体而言,该研究将RNA乙酰化修饰纳入“冷肿瘤”免疫调控框架,强调亚细胞分子稳态失衡在肿瘤免疫耐受中的关键意义,为开发联合表观修饰与免疫治疗策略提供了新的理论依据与干预方向。
作者信息
该研究由江南大学附属医院胡曙东、茆勇、胡浩担任通讯作者;Leisheng Wang为第一作者。