项目文章 | Cell:徐医大首篇,吕凌教授团队发现肿瘤产生的氨通过调节性T细胞代谢导致免疫抑制和治疗耐药
在肿瘤这一异质性代谢微环境中,代谢紊乱是其核心特征之一。为了维持高速增殖,肿瘤细胞通常表现出高度活跃的谷氨酰胺分解(Glutaminolysis),而这一过程的副产物——氨,会在微环境中大量积聚。长期以来,氨被认为是一种具有细胞毒性的代谢废物,能够诱导CD8+效应T细胞凋亡或进入耗竭状态,从而削弱抗肿瘤免疫。
然而,一个令人费解的现象是:在同样充满氨毒性的微环境里,Treg(调节性T细胞)不仅能够安然无恙,反而表现出更强的聚集能力和抑制功能。这种代谢适应性的差异究竟源于何处?Treg细胞是否进化出了一种独特的“排毒”或“利废”机制,使其能够将微环境中的代谢压力转化为自身功能的增益?

2026年1月,徐州医科大学附属医院吕凌教授与南京医科大学第一附属医院的古鉴教授研究团队系统揭示了肿瘤来源氨被Treg代谢利用,从而进一步抑制抗肿瘤免疫并促进免疫治疗耐药的关键机制。相关研究成果以“Tumor-produced ammonia is metabolized by regulatory T cells to further impede anti-tumor immunity”为题,在国际顶级期刊《Cell》见刊。
研究思路
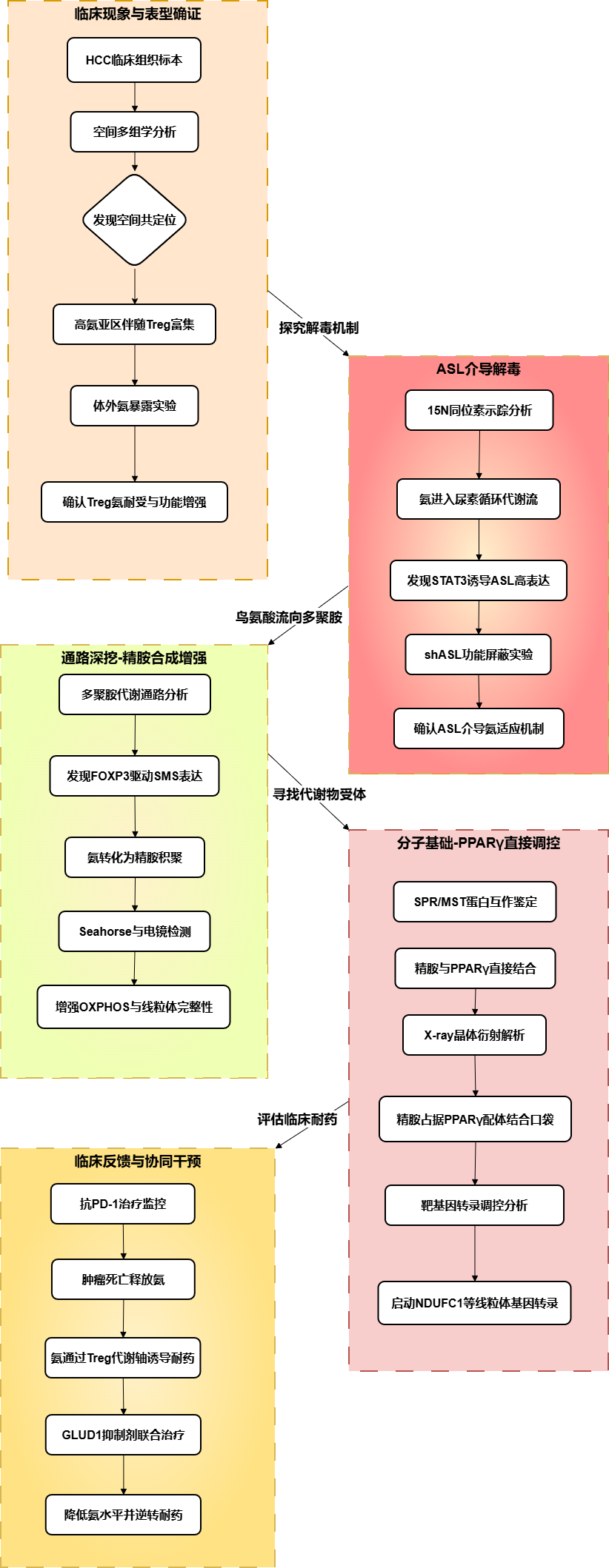
主要研究结果
1. 高谷氨酰胺分解亚区是诱导Treg细胞特异性富集的代谢微龛
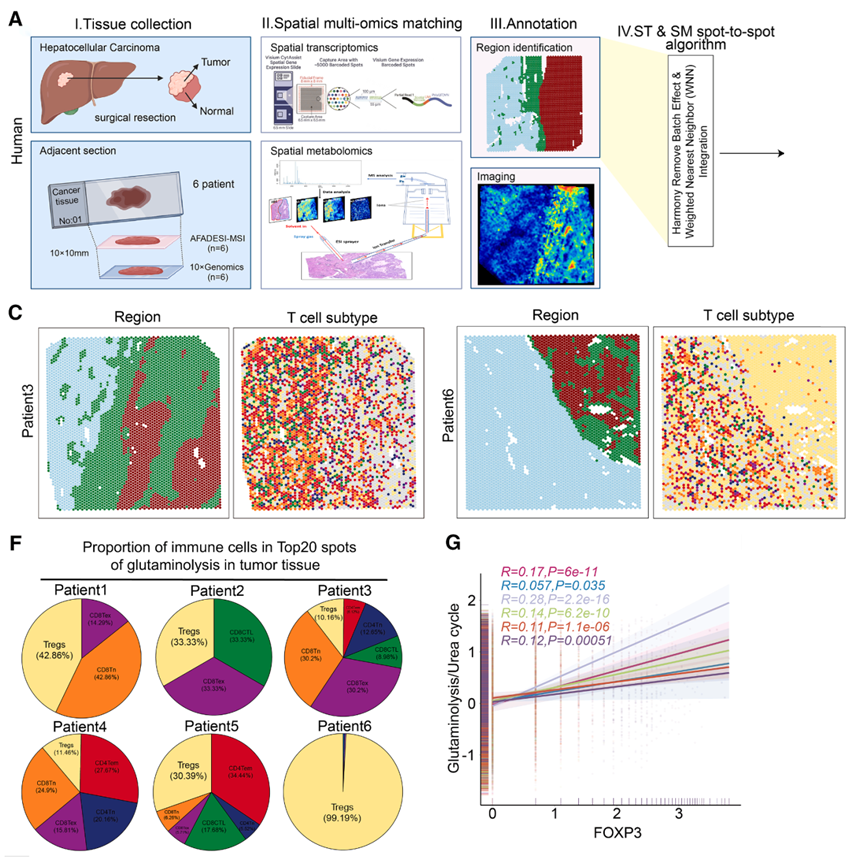
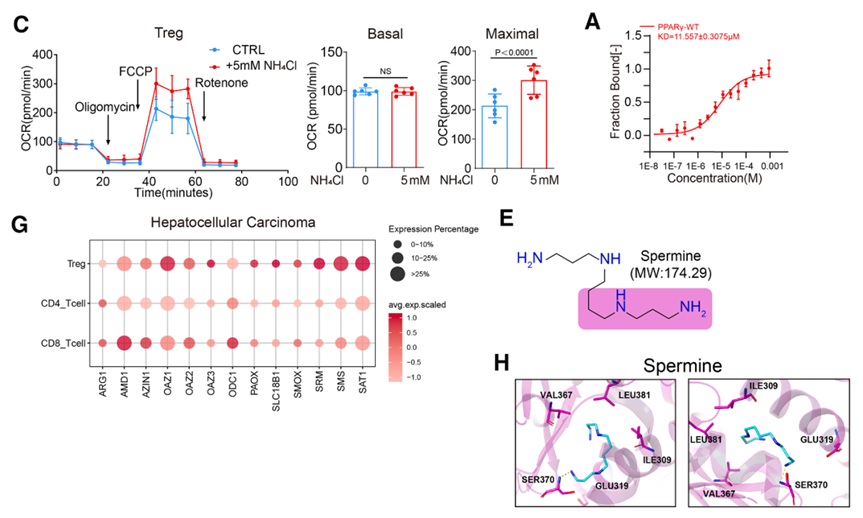
研究团队首先通过空间转录组学和空间代谢组学技术,对人肝细胞癌组织进行了高分辨率的制图分析。结果发现,肿瘤组织内部存在显著的代谢异质性。在谷氨酰胺分解活跃且尿素循环活动低下导致的氨积聚亚区,CD8+和CD4+效应T细胞的数量显著减少,甚至出现大量死亡,然而Treg细胞却在这些区域表现出异常的富集状态。进一步定量分析显示,在大部分高谷氨酰胺分解的位点中,Treg细胞都是最主要的免疫细胞群体,且其丰富度与氨代谢信号呈正相关。这表明,Treg细胞具有一种独特的代谢适应机制,使其能在高氨的严酷环境中生存并执行功能。
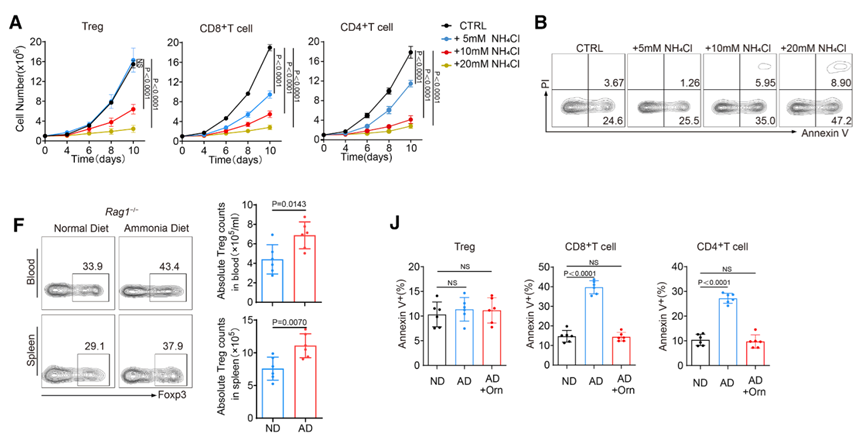
2. Treg细胞展现出卓越的氨毒性耐受力
为了验证Treg细胞在氨压力下的生存优势,研究团队在体外将不同T细胞亚群暴露于不同浓度的氯化铵(NH₄Cl)中。结果显示,5 mM浓度的氨即可显著抑制效应T细胞的增殖并诱导其大量凋亡,而Treg细胞在相同压力下不仅存活率更高,甚至上调了其免疫抑制分子(如PD-1和CTLA-4)的表达。在体内实验中,高氨饮食显著增加了荷瘤小鼠脾脏和血液中的Treg细胞频率。这些证据确凿地证明,氨对效应T细胞具有代谢毒性,却能通过特定的代谢通路增强Treg细胞的稳定性和抑制功能。
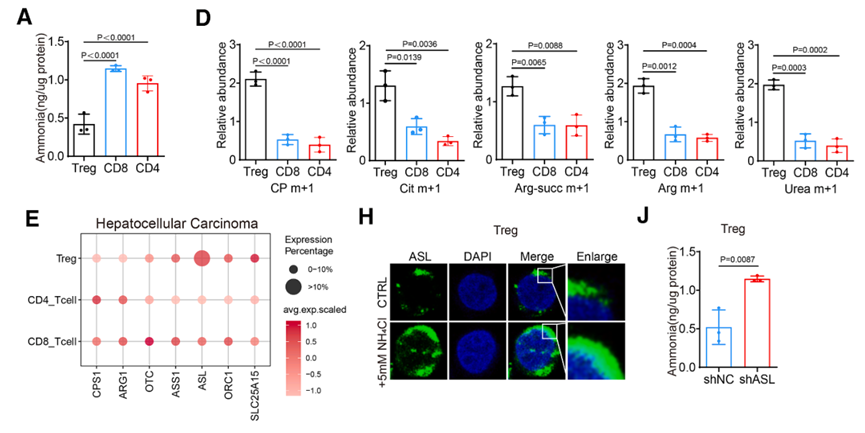
3. ASL介导的尿素循环开启氨解毒机制
为什么Treg细胞能抗氨毒?研究团队发现,Treg细胞在感知到氨压力后,会特异性地激活尿素循环通路。同位素示踪分析(¹⁵N-NH₄Cl)证实,Treg细胞对氨的利用率显著高于其他T细胞。机制研究锁定在ASL上:在氨的刺激下,Treg细胞并非通过经典磷酸化路径,而是诱导共激活因子SRC3与STAT3直接结合,形成转录复合物大幅上调ASL的表达,从而将毒性的氨转化为无毒的尿素循环中间产物。当使用shRNA沉默ASL后,Treg细胞内部氨水平升高,其生存优势和抑制功能随之消失,证明了尿素循环是其排毒的关键支柱。
4. 精胺直接绑定PPARγ激活线粒体代谢能量
除了排毒,尿素循环产生的中间产物鸟氨酸(Ornithine)成为了连接排毒与增益的桥梁。氨在Treg内经由ASL等酶处理后,进一步通过FOXP3驱动的精胺合成酶转化为精胺(Spermine)。由于外源精胺无法直接进入Treg细胞,这种胞内自给自足的代谢模式成为了其谱系特异性的适应机制。而且研究团队通过晶体结构解析发现,精胺能直接结合在核受体PPARγ的配体结合口袋中。这种结合促进了线粒体复合物相关基因的转录,从而大幅增强了Treg的氧化磷酸化水平和线粒体完整性。利用Ribo-seq技术(由表观生物提供),研究团队进一步证实,这种线粒体能量水平的跃升,本质上是为了支持 FOXP3等核心免疫抑制分子的翻译效率,确保其蛋白水平的稳定产出。这套“精胺-PPARγ-线粒体”轴,是Treg细胞在肿瘤环境中实现功能增益的关键代谢调节通路。
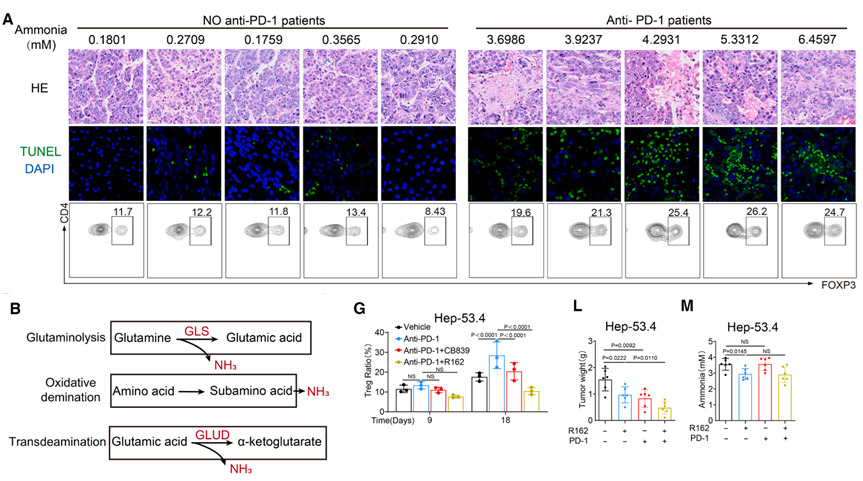
5. 抗PD-1引起的肿瘤死亡竟成了Treg细胞功能的增强底物
最后,研究团队探讨了这一代谢机制在临床耐药中的作用。在接受抗PD-1治疗的患者中,肿瘤细胞的凋亡通过GLUD1介导的转脱氨基作用释放了大量的氨。不同于常规认知的谷氨酰胺分解,抗PD-1导致的肿瘤凋亡主要通过GLUD1介导的转脱氨基作用释放氨。研究证实,常规GLS1抑制剂无法逆转PD-1耐药,而通过靶向GLUD1或Treg氨代谢通路联用抗PD-1,才能打破这种免疫抑制循环,降低Treg浸润,并大幅提升抗肿瘤效果。这一发现揭示了肿瘤死亡与免疫抑制之间隐秘的代谢反馈回路,为克服耐药提供了新靶点。
总结
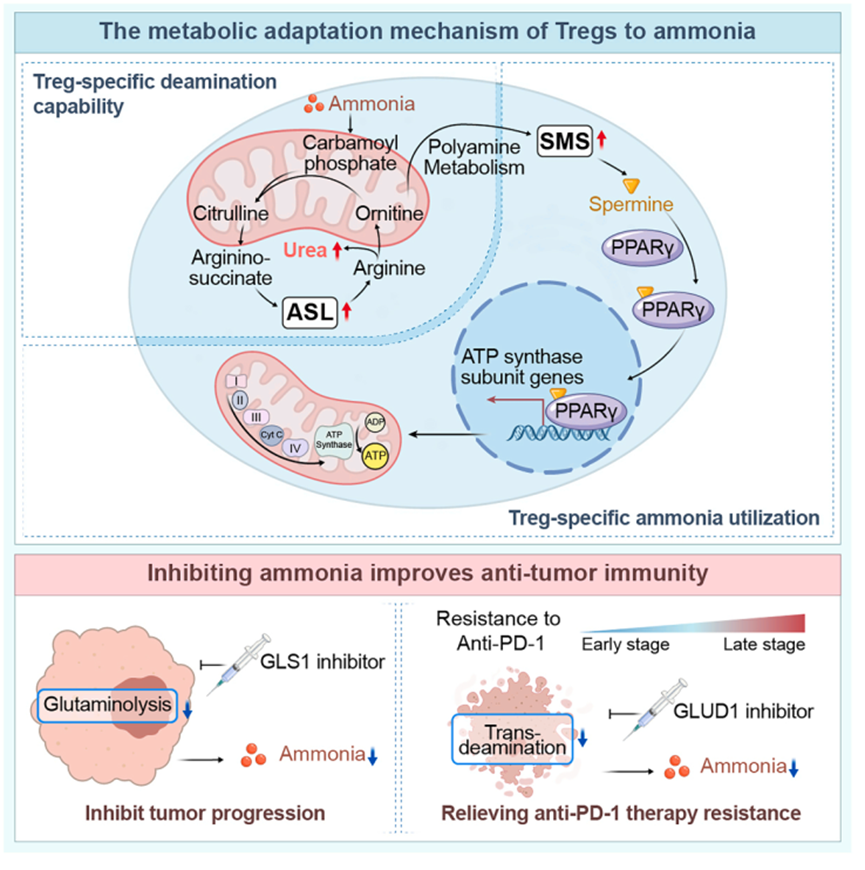
该研究打破了“氨仅是代谢废物”的传统认知,深入阐明了氨在调节性T细胞适应肿瘤微环境中的双重角色:既是生存挑战,也是功能增强的信号分子。研究首次确证了“氨-SMS-精胺-PPARγ-OXPHOS”这一精细的代谢触发链路,显示出Treg细胞在恶劣微环境中的谱系特异性代谢适应策略。
文章对免疫治疗耐药机制的探讨具有极高的临床启发性。抗PD-1治疗在诱导肿瘤细胞凋亡的同时,触发了由GLUD1介导的转脱氨基作用并释放大量氨,从而在代谢层面强化了抑制性Treg细胞的功能并诱导了免疫治疗耐药。这一发现提醒我们,抗肿瘤治疗需要考虑代谢产物对免疫图谱的二次改造。通过抑制GLUD1减少氨的产生,或靶向Treg细胞的氨代谢通路(如ASL、SMS),有望打破这种免疫抑制循环,为克服PD-1耐药提供切实可行的联合方案。
作者介绍
该研究由徐州医科大学附属医院吕凌教授担任主要通讯作者,南京医科大学第一附属医院肝胆中心古鉴教授为第一作者并兼任共同通讯作者;南京医科大学李彧、陈秋阳、宋子延和钱去非为共同第一作者。
- - - 推荐阅读 - - -

超级增强子项目 | SE驱动的lncRNA UNC5B-AS1通过调控乳酸化抑制肺动脉平滑肌细胞炎症表型转换
研究揭示了受超增强子调控的IncRNA UNC5B-AS1在缺氧时表达下调,通过减弱线粒体功能并增强糖酵解介导的组蛋白乳酸化,驱动肺动脉平滑肌细胞向炎症表型转换,而补充该RNA片段可有效缓解肺动脉高压进程
2026-01-29

客户文章 | Cancer Res(IF 16.6):SETD8通过调控线粒体稳态维持t(8;21)急性髓系白血病干细胞功能
表观生物为此提供CUT&Tag和ATAC-seq服务。
2026-01-08

多组学项目文章 | Adv Sci:Ythdc1-p300-Klf5复合物介导的高尔基体功能障碍促进主动脉瘤进展
表观生物为此提供ATAC-seq、 HiChiP、 GRO-seq
2025-12-26
