Cell Rep Med | DDX5超级增强子驱动鼻咽癌血管生成拟态形成:揭示抗血管生成治疗耐药新机制
抗血管生成疗法(AAT)在鼻咽癌等多种恶性肿瘤治疗中已被应用超过二十年,然而其临床疗效仍然有限。虽然靶向VEGF通路的抗血管生成药物(AAD)能够改善患者的无进展生存期和局部控制时间,但几乎所有患者都不可避免地会产生治疗耐药性,导致总体生存率未见显著提升。这种耐药现象的潜在机制一直是肿瘤治疗领域亟待解决的关键问题。
血管生成拟态(Vasculogenic Mimicry, VM)作为一种独立于内皮细胞和VEGF的新型肿瘤血液灌注系统,在多种高侵袭性和转移性恶性肿瘤中被发现,并与肿瘤转移和不良预后密切相关。VM由高度恶性的肿瘤细胞和基底膜形成,具有成熟的微循环功能,这可能解释了为什么VM对AAD不敏感。然而,VM形成在AAD耐药中的具体作用机制以及如何通过表观基因组学调控VM形成仍不清楚。这提出了一个关键问题:在抗血管生成治疗过程中,是否存在代偿性VM形成导致治疗耐药?其分子调控机制是什么?

2025年6月17日,南通大学附属医院耳鼻咽喉头颈外科研究所的游波团队在《Cell Reports Medicine》杂志上发表了一篇题为“DDX5 super-enhancer promotes vasculogenic mimicry formation and metastasis in nasopharyngeal carcinoma by enhancing ADAM10 transcription”的文章。该研究揭示了抗血管生成药物耐药的重要机制——代偿性血管生成拟态形成。研究团队采用DIA质谱蛋白质组学技术筛选出ADAM10作为促进VM形成的关键蛋白,发现其在转移性鼻咽癌患者外泌体中显著富集。通过CUT&Tag测序分析H3K27ac修饰识别超级增强子,结合Hi-C技术解析三维基因组结构,发现DDX5和E2F1两个转录因子通过远程环状相互作用被超级增强子激活,进而上调ADAM10表达。体内外实验证实,IM联合尼妥珠单抗能够同时抑制血管生成和VM形成,有效克服AADs耐药性,抑制鼻咽癌转移并改善预后。该研究为理解抗血管生成治疗耐药机制提供了新的表观遗传学视角,并提出了潜在的联合治疗策略。(CUT&Tag和Hi-C由表观生物提供)
研究技术路线图

关键研究结果
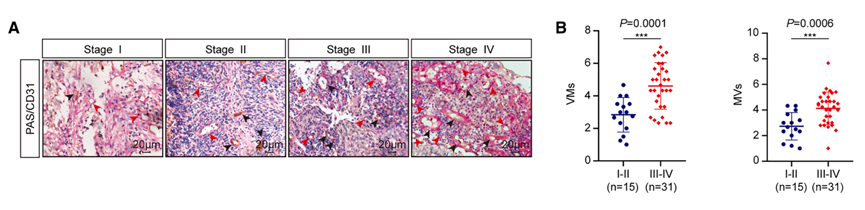
临床病理分析和动物模型研究共同揭示了VM在鼻咽癌进展和治疗耐药中的关键作用。通过PAS/CD31双染色技术成功区分了VM和MV两种微循环结构,统计分析显示晚期患者(III-IV期)的VMD和MVD均显著高于早期患者(I-II期)。
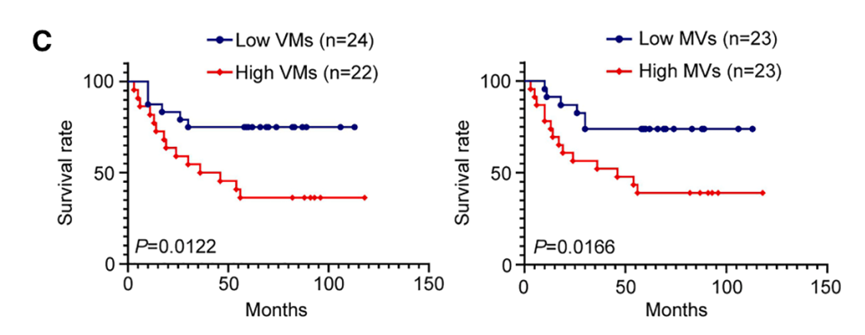
生存分析证实高VMD或高MVD的患者表现出更差的总体生存率。
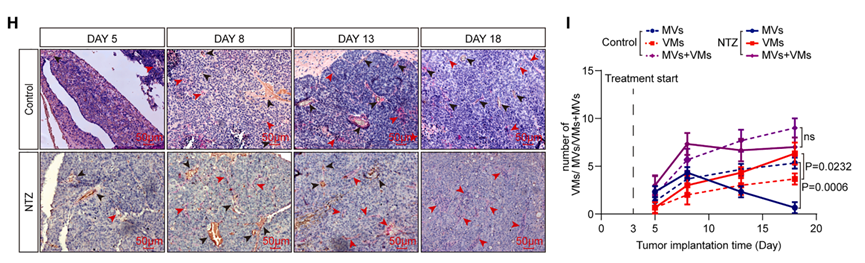
更重要的发现来自鼻咽癌原位移植小鼠模型的动态监测:尽管NTZ治疗未能显著抑制肿瘤生长或转移,但微循环系统分析发现MV密度下降的同时VM密度出现代偿性升高,使得总体血管密度保持稳定。这一现象首次在体内动态可视化了AAD治疗过程中的代偿性VM形成,为理解治疗耐药提供了直接证据,提示单纯靶向VEGF依赖性血管生成的局限性。
系统的功能分析确立了外泌体ADAM10在VM形成中的核心地位。体外研究显示高转移性细胞系形成的管状结构显著多于非转移性细胞系,经侵袭筛选获得的CNE2-T3细胞表现出更强的间质样形态和VM形成能力。关键发现是转移性患者血清外泌体能够诱导受体细胞形态转变、促进VM形成并增强迁移能力,其效应显著强于非转移性患者外泌体。
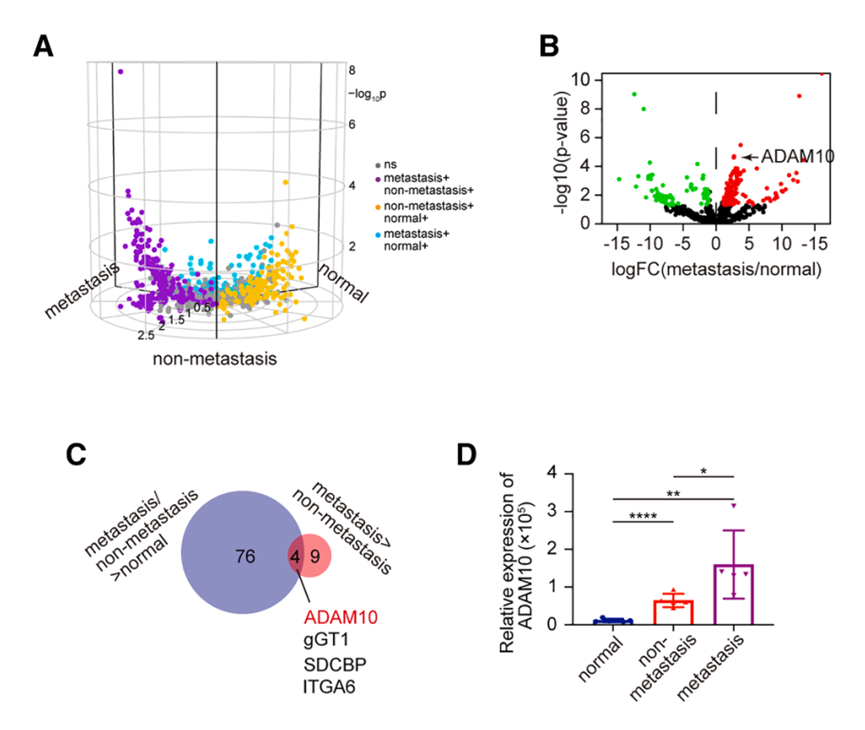
DIA质谱蛋白组学分析(每组6例)系统比较了不同来源外泌体的蛋白表达谱,在转移性外泌体特异性上调的蛋白中,ADAM10表现出最显著的差异性表达。
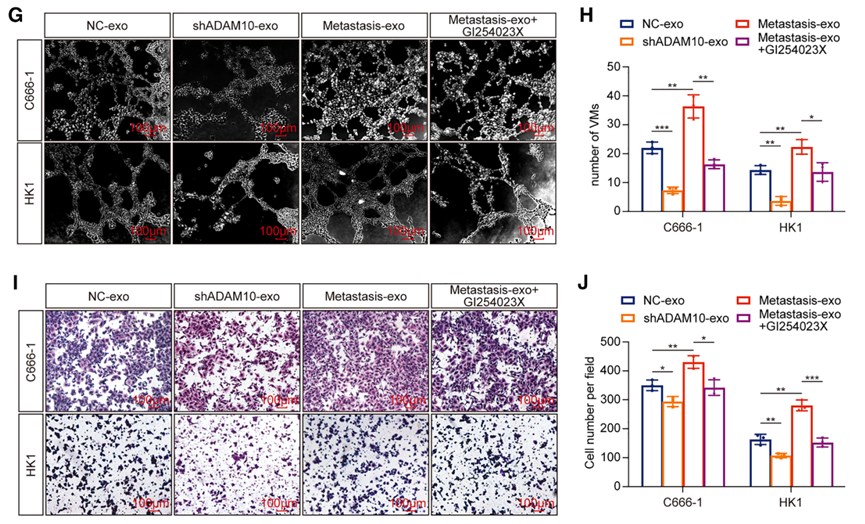
功能验证显示ADAM10敲低的细胞分泌的外泌体显著抑制受体细胞的VM形成、迁移和侵袭,而转移性外泌体增强这些恶性功能,ADAM10特异性抑制剂能够有效逆转外泌体的促进作用。这些结果揭示了外泌体介导的ADAM10水平转移在肿瘤微环境重塑和VM形成中的关键作用。
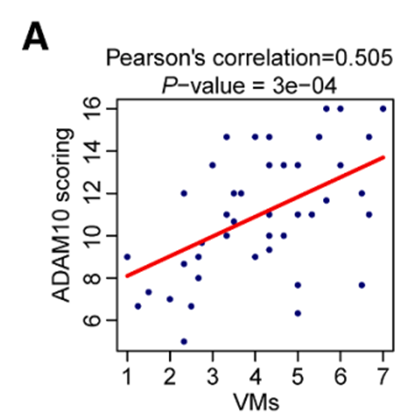
临床标本分析和功能实验系统验证了ADAM10在鼻咽癌进展中的驱动作用。免疫组化分析显示ADAM10高表达与晚期临床分期和不良预后相关,ADAM10表达水平与VMD呈显著正相关。
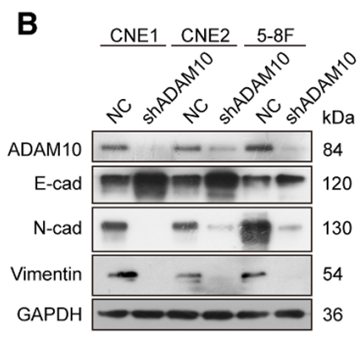
体外功能研究证实ADAM10敲低显著抑制EMT进程、VM形成、迁移和侵袭能力。
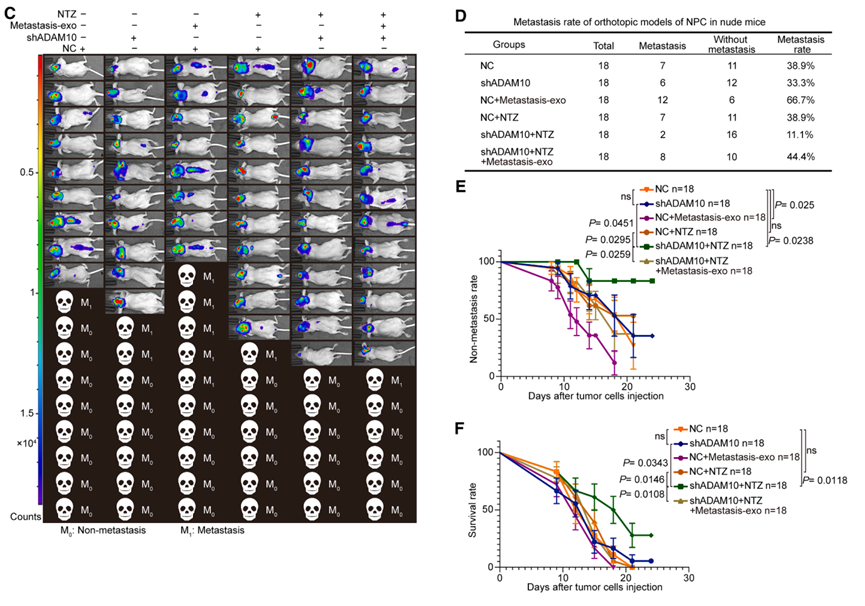
原位移植模型的系统评估揭示了联合治疗的关键价值:单独NTZ治疗或ADAM10敲低均未显著抑制肿瘤生长,但ADAM10敲低联合NTZ治疗产生了显著的协同抗肿瘤效应,表现出最高的生存率和最低的转移率。
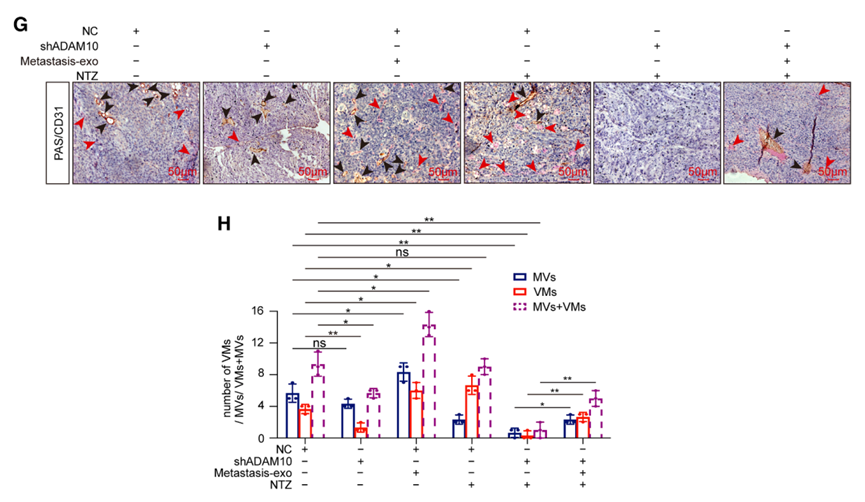
微循环系统分析阐明了作用机制:转移性外泌体同时富集MV和VM;NTZ单药降低MVD但导致VMD代偿性升高;ADAM10敲低单独使用降低VMD并适度降低MVD;而联合治疗有效抑制EMT、ADAM10表达以及MV和VM双重微循环系统,证实了通过同时靶向两种血液供应通路克服AAD耐药的可行性。
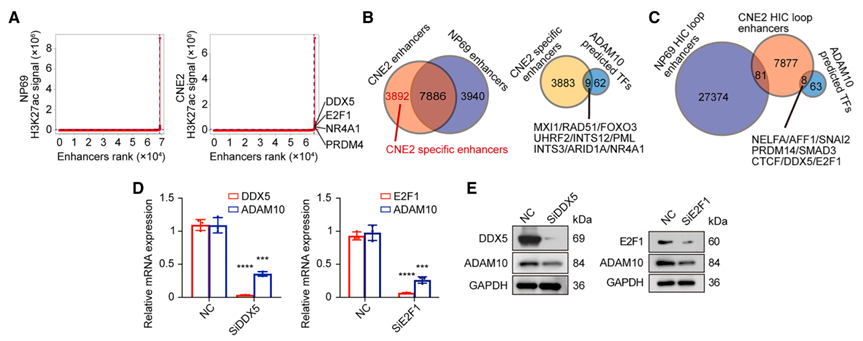
表观基因组学分析揭示了ADAM10转录上调的多层次调控机制。H3K27ac CUT&Tag测序显示ADAM10未直接关联超级增强子,Hi-C分析也未发现其与远端增强子的直接相互作用,提示通过转录因子介导的间接调控。整合分析筛选出候选转录因子,功能验证显示只有DDX5和E2F1的敲低能够显著降低ADAM10表达。
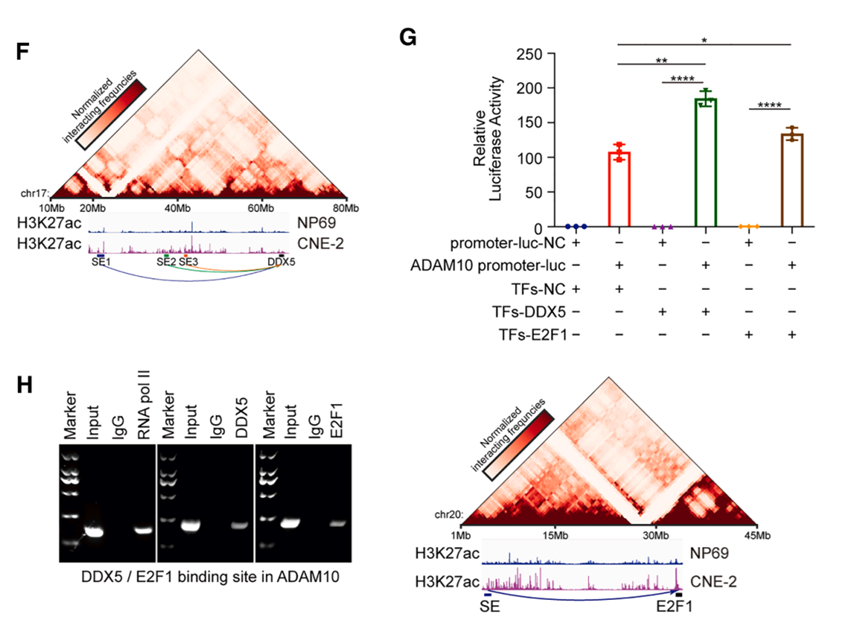
Hi-C数据揭示了CNE2特异性的长程染色质相互作用:超级增强子区域与DDX5和E2F1的启动子区域形成远程环状结构。荧光素酶报告基因和ChIP实验证实DDX5和E2F1能够结合ADAM10启动子并增强其转录活性。
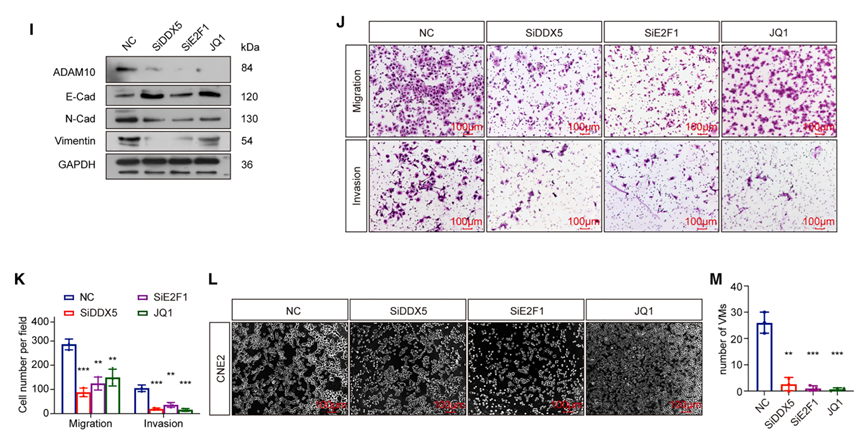
DDX5或E2F1敲低以及BET抑制剂JQ1处理均导致ADAM10表达下降,并抑制EMT、迁移、侵袭和VM形成。这一"超级增强子-转录因子-效应基因"三级调控轴的发现,不仅阐明了ADAM10上调的表观遗传基础,也为理解肿瘤细胞如何通过重编程染色质结构获得恶性表型提供了范例。
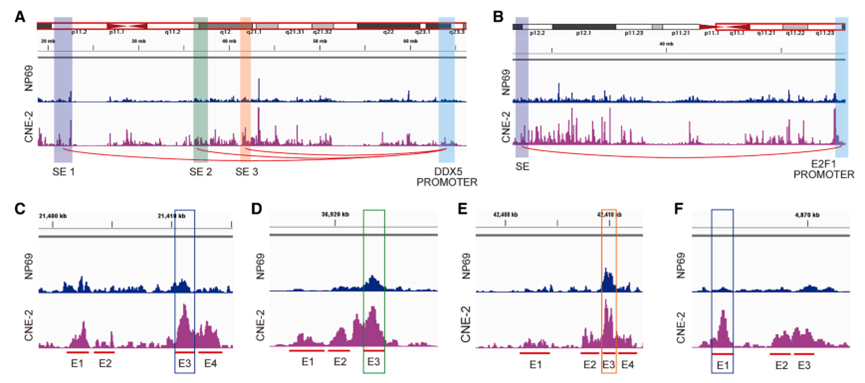
为精确解析超级增强子功能,研究采用CRISPR-Cas9技术分别删除DDX5和E2F1超级增强子的关键组分。
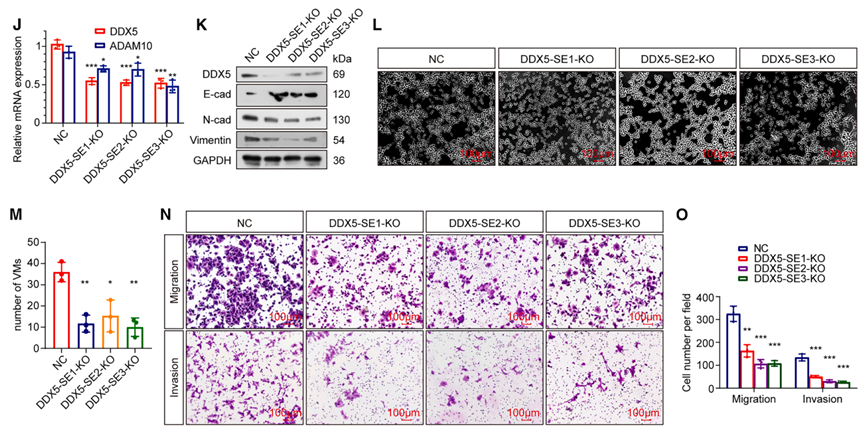
DDX5三个超级增强子关键组分任一删除均显著降低DDX5和ADAM10表达,抑制EMT、迁移、侵袭和VM形成;而E2F1超级增强子删除无明显效应,突显了DDX5超级增强子的核心调控地位。
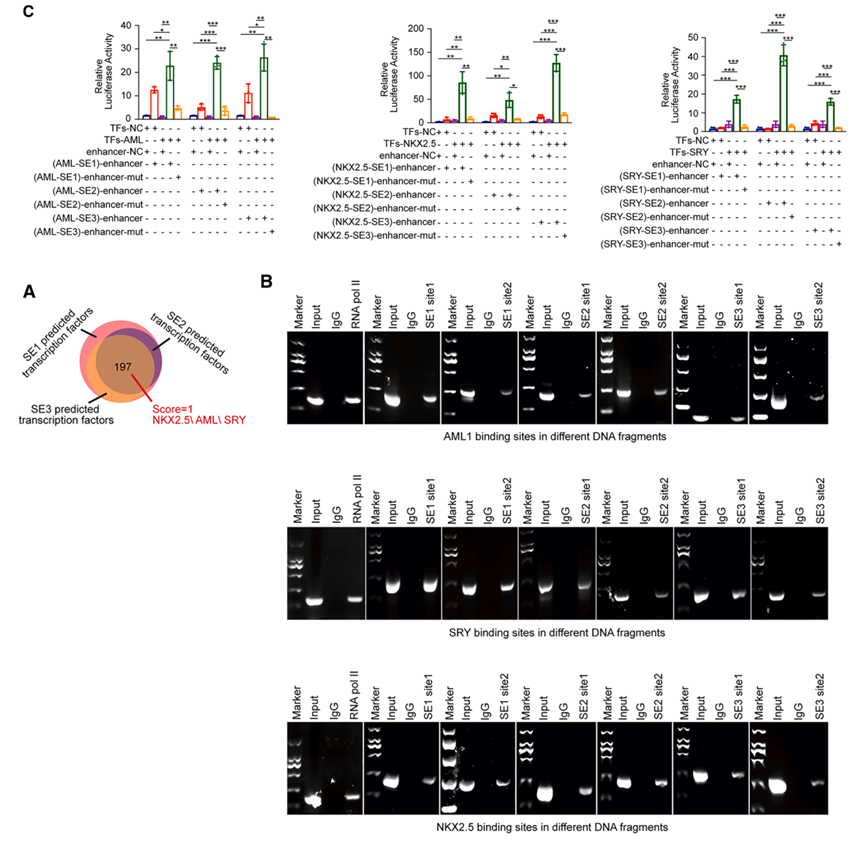
转录因子筛选发现NKX2.5、AML和SRY结合评分最高,ChIP和荧光素酶实验证实它们结合DDX5超级增强子关键组分并激活转录。
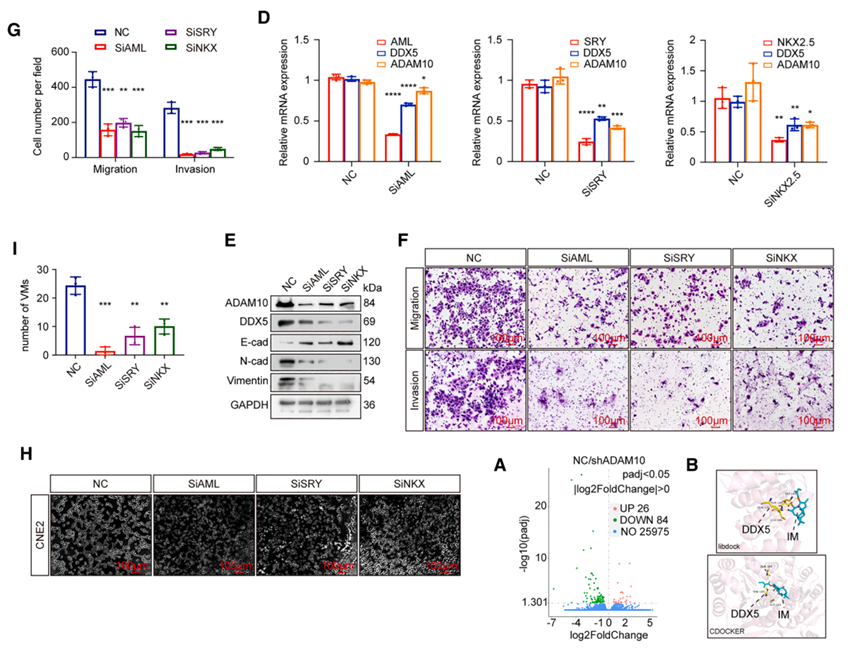
这三个转录因子在鼻咽癌组织和高侵袭性细胞中表达上调,其敲低均导致DDX5和ADAM10下调并抑制恶性功能。基于完整调控网络,研究通过转录组学和虚拟筛选发现ingenol mebutate与DDX5具有优异结合能力。
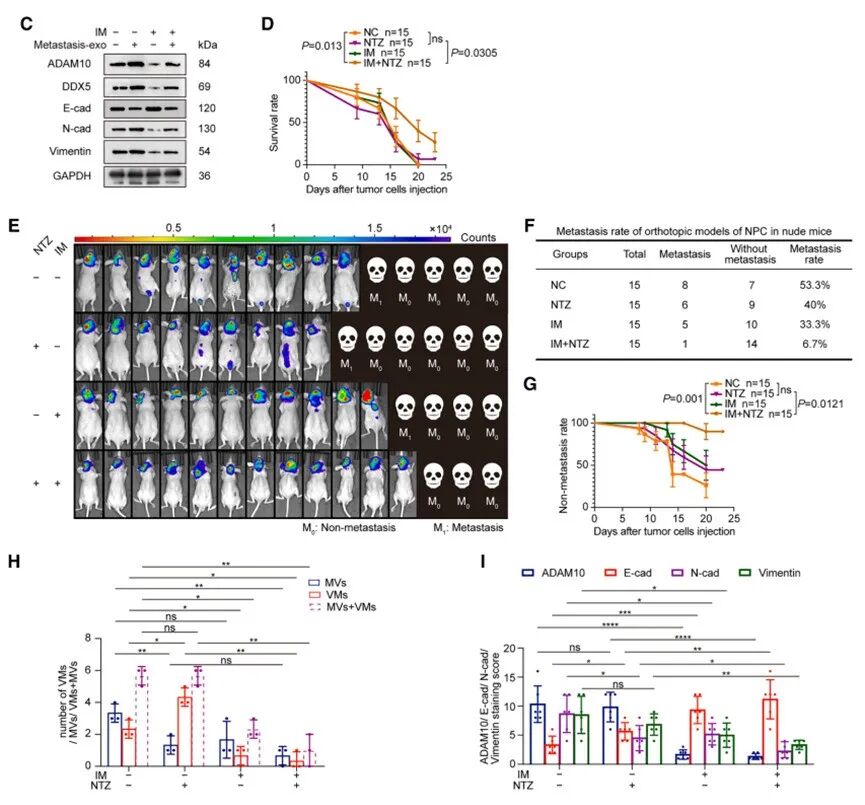
体外实验证实IM降低DDX5和ADAM10表达,抑制VM形成和迁移。在原位移植模型中,IM联合NTZ治疗显著改善生存率、降低转移率,同时抑制MVD和VMD,为AADs耐药患者提供了潜在的治疗选择。
总结
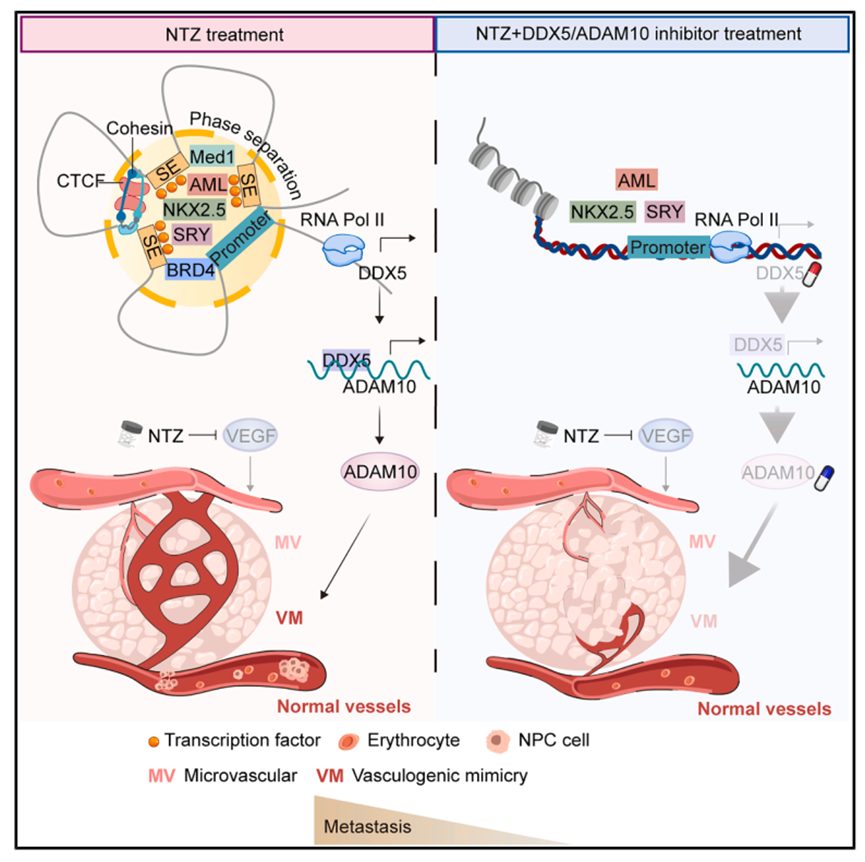
研究揭示了鼻咽癌抗血管生成治疗耐药的核心机制,发现AAD治疗导致传统血管减少的同时诱导血管生成拟态代偿性增加。转移性患者血清外泌体富集的ADAM10通过"教育"受体细胞促进VM形成。表观遗传学分析揭示了NKX2.5/AML/SRY-DDX5超级增强子-ADAM10的三级转录调控轴,其中DDX5超级增强子发挥核心作用。基于此机制,研究提出"双重靶向微循环"策略,发现ingenol mebutate联合AAD能同时抑制VM和MV,显著改善生存并降低转移。这一"老药新用"策略为克服AAD耐药提供了理论基础和潜在治疗方案,具有重要临床转化价值,但仍需在免疫健全模型中验证并评估IM的特异性和安全性。
- - - 推荐阅读 - - -

项目文章 | Cell:徐医大首篇,吕凌教授团队发现肿瘤产生的氨通过调节性T细胞代谢导致免疫抑制和治疗耐药
表观生物为此提供Ribo-seq、RNA-seq服务
2026-02-06

超级增强子项目 | SE驱动的lncRNA UNC5B-AS1通过调控乳酸化抑制肺动脉平滑肌细胞炎症表型转换
研究揭示了受超增强子调控的IncRNA UNC5B-AS1在缺氧时表达下调,通过减弱线粒体功能并增强糖酵解介导的组蛋白乳酸化,驱动肺动脉平滑肌细胞向炎症表型转换,而补充该RNA片段可有效缓解肺动脉高压进程
2026-01-29

客户文章 | Cancer Res(IF 16.6):SETD8通过调控线粒体稳态维持t(8;21)急性髓系白血病干细胞功能
表观生物为此提供CUT&Tag和ATAC-seq服务。
2026-01-08
