超级增强子项目 | SE驱动的lncRNA UNC5B-AS1通过调控乳酸化抑制肺动脉平滑肌细胞炎症表型转换
肺动脉高压(Pulmonary hypertension,PH)的核心病理基础之一是低氧诱导的肺动脉平滑肌细胞(PASMC)表型转变,尤其是向炎症表型的转化,但其上游转录调控与代谢—表观遗传耦联机制尚不清楚。既往研究已知提示超级增强子是驱动细胞身份关键基因表达的核心调节元件,而低氧条件下超级增强子驱动的长链非编码RNA是否参与PASMCs炎症性表型重塑仍缺乏系统研究;与此同时,乳酸及其介导的组蛋白乳酰化被认为是连接代谢重编程与炎症基因转录的重要新型表观遗传机制,但其在肺血管重塑中的功能尚未明确。因此,阐明低氧环境下超级增强子(SE)—lncRNA轴如何通过代谢与乳酰化调控PASMCs炎症表型转变,是理解肺动脉高压发生机制并探索新型干预靶点的关键科学问题。

研究亮点
- SE调控的lncRNA UNC5B-AS1,在缺氧的肺动脉平滑肌细胞中表达下调,并参与肺血管重构的调控。SE通过形成染色质loop,将转录因子FOXP3招募至UNC5B-AS1的启动子区域,从而调控其表达。在线粒体中,由SE驱动表达的UNC5B-AS1可作为分子支架,LRPPRC(稳定富含亮氨酸的PPR基序蛋白)与线粒体复合物Ⅳ之间的相互作用,进而影响线粒体代谢。在细胞质中,缺氧状态下UNC5B-AS1调控的乳酸生成与糖酵解激活,会诱导IL-1β、IL-6以及TNF-α启动子区的H3K18la,最终促使肺动脉平滑肌细胞向炎症表型转化。
- 体内实验显示,过表达UNC5B-AS1的保守片段可缓解肺动脉高压。
技术路线/研究设计
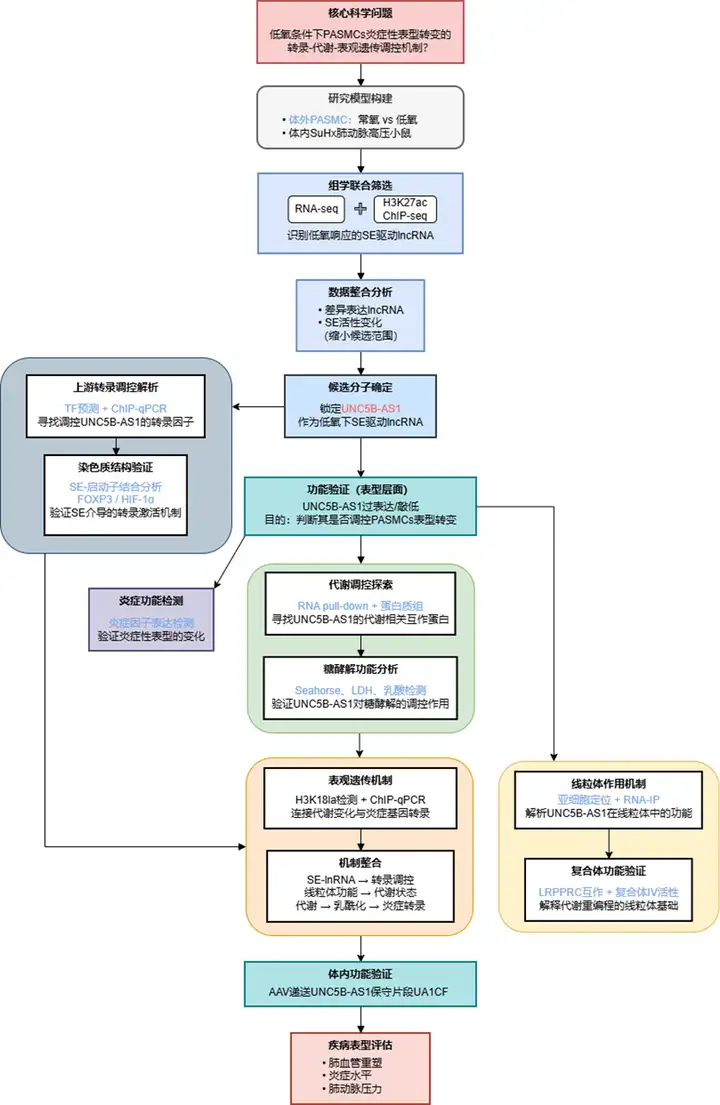
研究结果
1. SE驱动的UNC5B-AS1在缺氧环境下显著下调
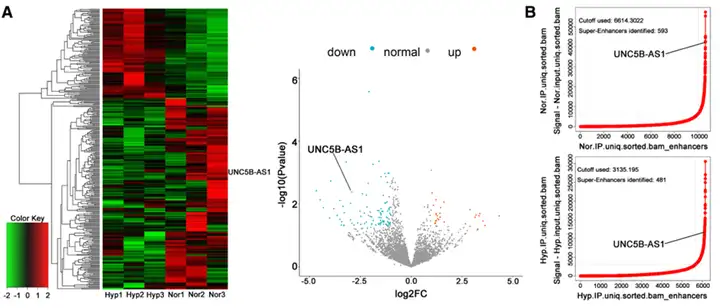
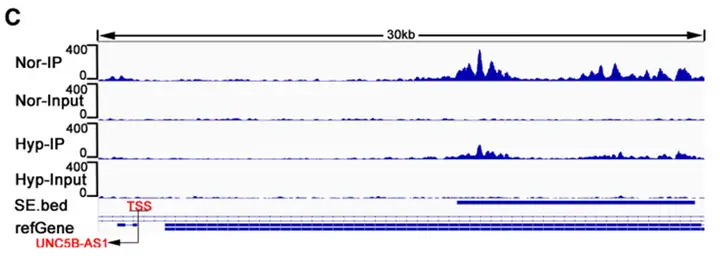
RNA-seq分析结果显示,在低氧处理的PASMC中,多条lncRNA出现显著表达变化(A),其中UNC5B-AS1下调幅度最为明显。结合H3K27ac ChIP-seq数据,研究进一步鉴定出低氧条件下活性发生改变的SE(B、C),UNC5B-AS1位点上游的SE区域H3K27ac信号显著减弱。
通过SE典型抑制实验(BET抑制剂JQ1与CDK7抑制剂处理),UNC5B-AS1表达明显下降,证实其转录依赖SE活性。RNA FISH结果显示,UNC5B-AS1主要定位于细胞质,在低氧条件下信号显著减弱,从空间定位和表达层面共同确立其作为低氧响应SE驱动lncRNA的分子特征。
2. SE通过FOXP3介导染色质loop结构调控UNC5B-AS1转录
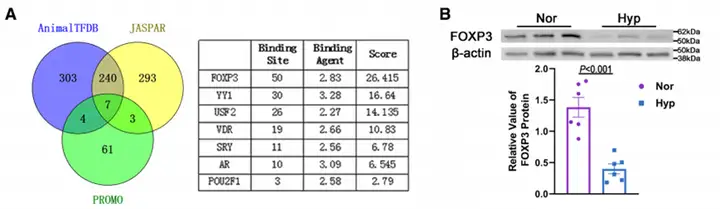
转录因子富集分析结果提示FOXP3是UNC5B-AS1上游潜在关键调控因子。ChIP-qPCR结果证实,FOXP3显著富集于UNC5B-AS1相关SE区域,并在低氧条件下结合能力下降。
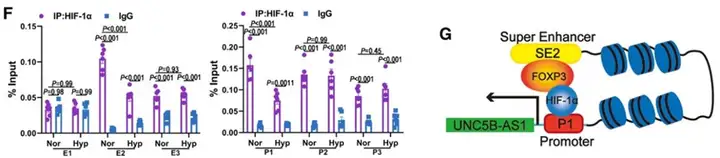
进一步分析显示,FOXP3与HIF-1α共同参与SE与UNC5B-AS1启动子之间的染色质互作。敲低FOXP3或干扰HIF-1α均可显著抑制UNC5B-AS1的转录水平(F、G),提示SE–FOXP3–HIF-1α轴是维持UNC5B-AS1表达的关键转录调控机制。
3. UNC5B-AS1抑制PASMC向炎症性表型转变
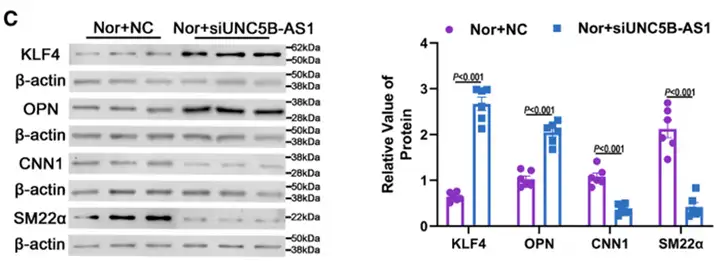
通过在PASMC中进行UNC5B-AS1过表达和敲低实验,研究系统评估其对细胞表型的调控作用。UNC5B-AS1过表达显著抑制低氧诱导的表型转变,下调合成/炎症相关标志物KLF4和OPN,并维持收缩型标志物CNN1和SM22α的表达。
相反,敲低UNC5B-AS1即使在常氧条件下亦可诱导PASMC炎症性表型特征,并显著上调IL-1β、IL-6和TNF-α的表达水平,提示UNC5B-AS1是抑制PASMC炎症性重编程的重要内源性因子。
4. UNC5B-AS1通过调控糖酵解与乳酸生成影响蛋白乳酸化
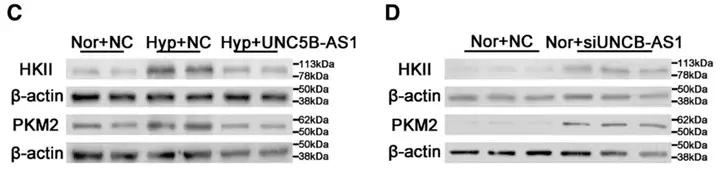
RNA pull-down联合质谱分析鉴定出多种与UNC5B-AS1互作的代谢相关蛋白,其中包括关键糖酵解酶PKM2、GAPDH和LDHA。功能实验显示,UNC5B-AS1过表达显著降低低氧PASMC的糖酵解水平和乳酸生成。
进一步检测发现,UNC5B-AS1显著抑制全蛋白乳酰化水平,并降低炎症相关基因启动子区域的H3K18la富集。ChIP-qPCR结果表明,IL-1β、IL-6和TNF-α启动子上的H3K18la信号显著减少,从而限制其转录激活。
5. UNC5B-AS1在线粒体中作为分子支架维持呼吸链复合体IV功能
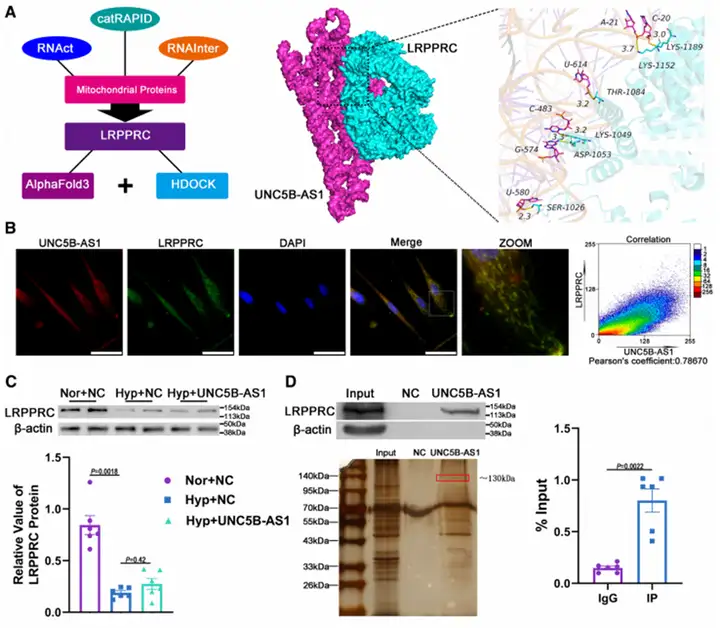
亚细胞分离与RNA定位实验显示,UNC5B-AS1部分定位于线粒体(A、B)。RNA IP和pull-down实验证实,UNC5B-AS1可直接结合LRPPRC(C、D)。
功能上,UNC5B-AS1促进LRPPRC与线粒体呼吸链复合体IV的稳定互作。敲低 UNC5B-AS1显著降低复合体IV活性和氧化磷酸化水平,并促使代谢偏向糖酵解,从线粒体功能层面解释其代谢调控作用。
6. UNC5B-AS1保守功能片段在体内缓解肺动脉高压进展
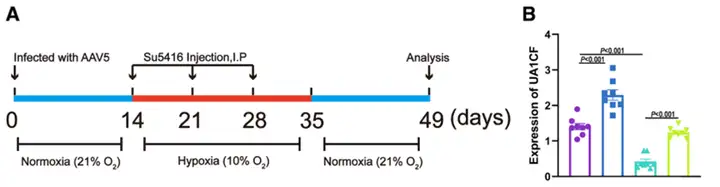
在SuHx诱导的肺动脉高压小鼠模型中,AAV介导的UNC5B-AS1保守功能片段UA1CF递送显著降低右心室收缩压和右心室肥厚指数,并明显改善肺血管壁增厚和血管重塑。
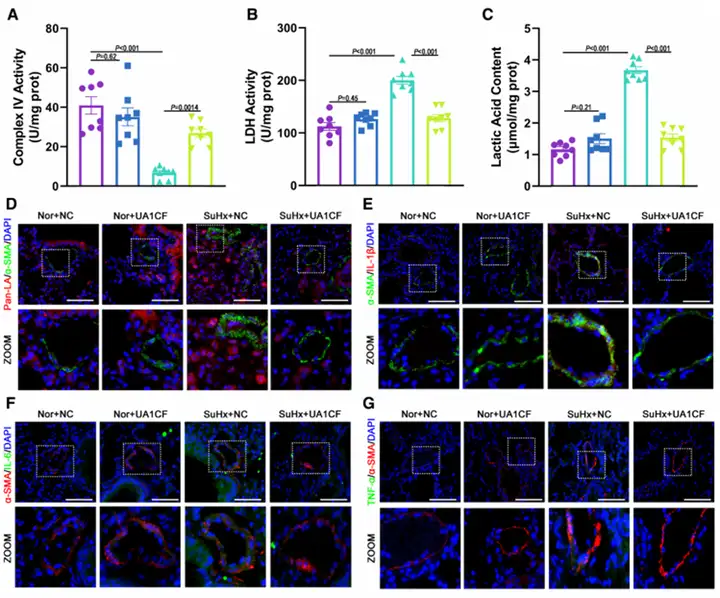
机制层面,UA1CF恢复肺组织中线粒体复合体IV活性,降低乳酸积累和蛋白乳酸化水平(A–C),并显著抑制炎症因子IL-1β、IL-6和TNF-α的表达。上述保护作用在雌雄小鼠中均得到一致验证。
小 结
低氧相关血管重塑的研究不应局限于单一信号通路或转录因子,而需要从染色质调控结构(如超级增强子)—非编码RNA—代谢状态—表观遗传修饰的整体调控网络出发进行系统解析。UNC5B-AS1的发现提示,具有细胞类型特异性的SE驱动lncRNA可能是连接代谢重编程与炎症转录的重要调控节点,值得在其他低氧相关疾病模型中进行系统筛选与功能验证。此外,该研究将组蛋白乳酰化引入肺血管重塑领域,也为探索不同代谢产物介导的表观遗传修饰及其疾病特异性调控机制提供了新的研究方向。
- - - 推荐阅读 - - -

客户文章 | Cancer Res(IF 16.6):SETD8通过调控线粒体稳态维持t(8;21)急性髓系白血病干细胞功能
表观生物为此提供CUT&Tag和ATAC-seq服务。
2026-01-08

多组学项目文章 | Adv Sci:Ythdc1-p300-Klf5复合物介导的高尔基体功能障碍促进主动脉瘤进展
表观生物为此提供ATAC-seq、 HiChiP、 GRO-seq
2025-12-26

m7G项目文章 | IF 20.6 中大附一团队揭示METTL1介导m7G修饰通过CTSB促进类风湿关节炎滑膜侵袭的分子机制
该研究首次揭示类风湿关节炎患者滑膜中METTL1表达升高,通过介导CTSB(组织蛋白酶B)mRNA内部m7G甲基化修饰增强其翻译效率,进而促进滑膜成纤维样细胞迁移和侵袭能力,驱动关节破坏
2025-12-11
