Science | 非结构化转录因子相互作用驱动基因组结合特异性的涌现
背景
数十年来,转录因子的基因组结合特异性被归因于其结构化DNA结合域(DBD)对特定序列基序的识别。然而,这一经典模型与大量实验证据存在根本性矛盾:真核基因组中潜在结合位点数量远超实际占据位点;具有相同序列偏好的不同TF往往定位于截然不同的基因组区域;而许多实际被占据的位点甚至缺乏可识别的结合基序。这些现象表明,仅凭DBD的序列识别能力无法充分解释TF的基因组定位逻辑。
与原核TF不同,真核TF普遍含有大量固有无序区域(IDR),这些区域不折叠成稳定的三维结构,而是参与多价、低亲和力的相互作用。尽管已有研究提示IDR影响TF的基因组占据模式,但相关结论主要依赖于测序技术对DNA切割信号的间接推断,而以往的成像研究又多涉及异位过表达或人工多聚化等实验干预,可能严重扭曲IDR的真实行为。因此,IDR在活细胞中如何影响TF的染色质结合与基因组定位,至今仍不清晰。

2026年3月19日,加州大学伯克利分校分子与细胞生物学系的Robert Tjian与Thomas G. W. Graham团队联合霍华德·休斯医学研究所于《Science》发表了题为Unstructured transcription factor interactions enable emergent specificity的研究。研究者采用邻近辅助光激活技术(PAPA)作为单分子蛋白质相互作用传感器,在活细胞中系统研究了IDR对TF相互作用及染色质结合的影响。核心发现包括:Sp1的DBD单独存在时与染色质结合能力极弱,且无法与全长Sp1共定位;而将IDR与各类无关DBD融合后,可显著增强其与Sp1的相互作用;在果蝇唾液腺活体成像中,将IDR融合至非特异性DBD可使其获得明确的基因座特异性定位。研究者据此提出,TF特异性并非由DBD单独决定,而是在染色质上通过多种无序相互作用的集体协同涌现而来。
研究路线

技术平台构建与核心检测方法
主研究的核心技术依托两个相互配合的平台。其一是自主搭建的斜线扫描(OLS)显微镜,支持宽视野单分子成像,实现高通量数据采集。其二是PAPA技术:将目标蛋白分别标记Halo-JF549(发送体)和SNAPf-JFX650(接收体),通过绿光激发发送体后选择性地重激活邻近接收体,从而在活细胞中直接检测蛋白质间的瞬时接近;405 nm紫光直接重激活作为内部对照,计算邻近指数(proximity index)以量化特异性相互作用。为确保生理相关性,研究者通过Cas9基因组编辑在内源Sp1位点插入HaloTag,并将SNAPf标记的转基因整合至AAVS1安全港位点,流式细胞术验证转基因表达量与内源Sp1相当。
2.1 Sp1 DBD单独存在时染色质结合严重受损,且无法与全长Sp1共定位
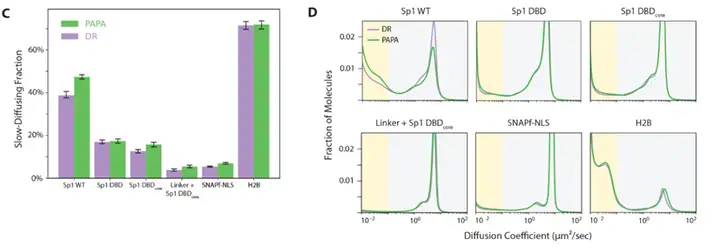
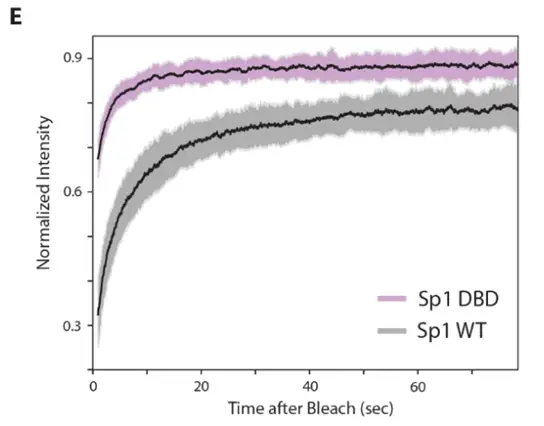
去除N端IDR的Sp1变体染色质结合比例从野生型的39%骤降至17%,而仅保留DBD的变体进一步降至13%。即便在DBD与SNAPf之间插入与N端IDR等长的柔性亲水接头,染色质结合仍几乎完全丧失。FRAP实验独立验证了这一结论,DBD单独存在时漂白深度明显更浅、恢复更快。
PAPA检测显示,DBD变体与全长Sp1的邻近指数与阴性对照H2B无法区分,表明DBD单独存在时既不能稳定结合染色质,也不能与全长Sp1共定位。
2.2 DBD侧翼的碱性无序区通过静电作用稳定染色质结合
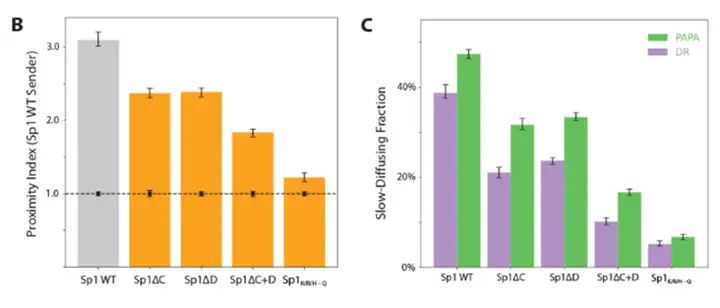
分别删除DBD两侧的碱性富集区C区或D区均导致染色质结合下降和与野生型Sp1相互作用减弱,双缺失(Sp1ΔC+D)效果叠加。将IDR中所有赖氨酸、精氨酸和组氨酸替换为谷氨酰胺导致染色质结合完全丧失,与野生型Sp1的相互作用也降至极低水平。
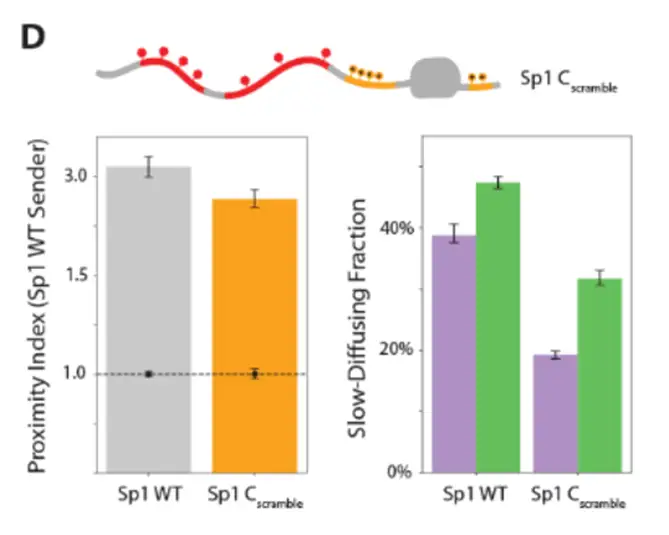
打乱C区序列在保持氨基酸组成不变的前提下增加了碱性残基与DBD的平均距离,导致染色质结合显著下降,提示碱性残基的空间分布而非单纯数量决定其功能。
2.3 无序区的自相互作用依赖于芳香族残基的数量与排列
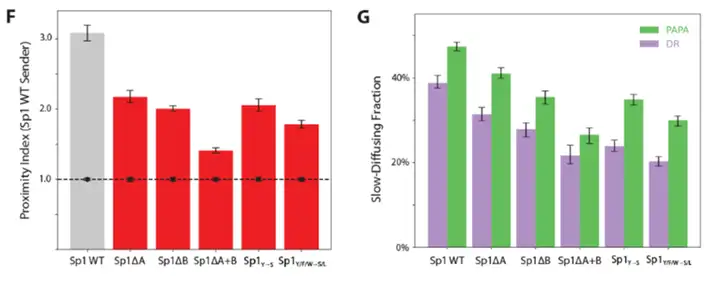
删除N端IDR中富含谷氨酰胺和芳香族残基的A区或B区,均导致染色质结合下降和与野生型Sp1相互作用减弱。将IDR外所有酪氨酸替换为丝氨酸或所有芳香族残基替换为非芳香族残基,均显著降低染色质结合和同型相互作用,且后者效果更强,表明同型相互作用强度与芳香族残基总量正相关。
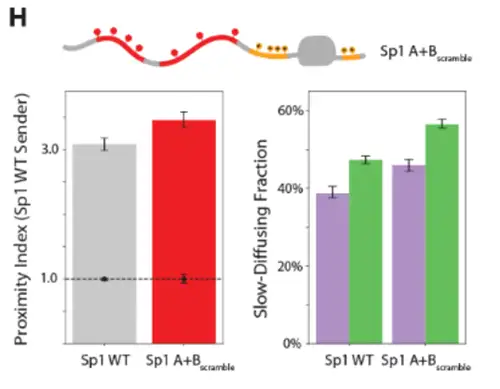
而且打乱A+B区序列在保持残基组成不变的情况下反而增强了与野生型Sp1的相互作用,说明IDR的相互作用特性对序列重排具有较强耐受性,甚至可因重排而增强。
2.4 弱DNA结合可稳定无序TF相互作用,且相互作用独立于序列特异性
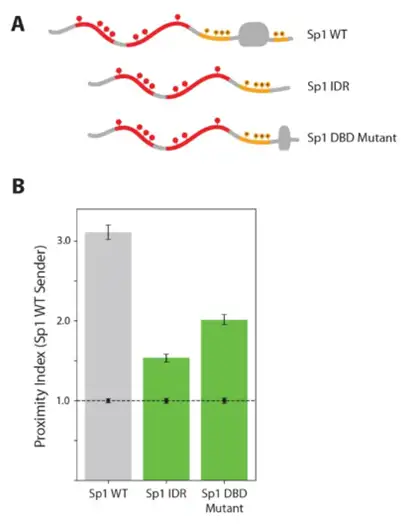
孤立的Sp1 N端IDR仅保留与野生型Sp1的弱相互作用。一个保留N端IDR但DBD被截短为单个锌指的疾病相关Sp1变体与野生型Sp1的相互作用显著强于孤立IDR,表明即使是弱的、非特异性DNA接触也能稳定无序TF相互作用。
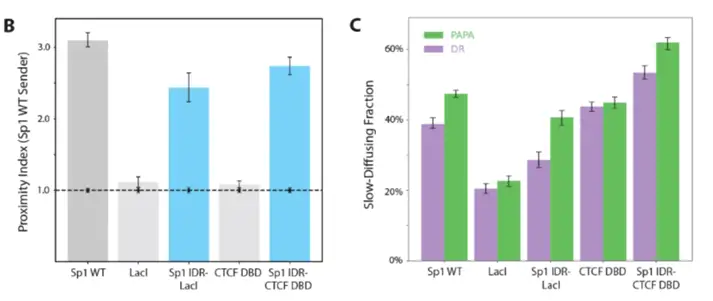
将Sp1 DBD替换为CTCF DBD或LacI(后者在人类细胞中无同源序列)构建的嵌合体,均比孤立IDR或孤立DBD表现出更强的与野生型Sp1的共定位,且PAPA重激活分子富集于染色质结合状态。这表明结构化DNA结合可稳定无序相互作用,且该效应不严格依赖于DBD的序列偏好。
2.5 基因组测序方法与活细胞成像结果存在系统性偏差
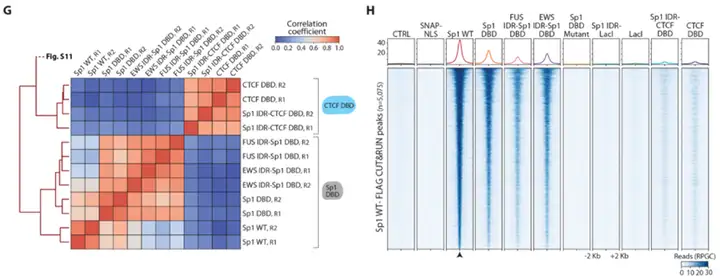
CUT&RUN显示全长Sp1与孤立Sp1 DBD产生高度重叠的基因组结合峰,暗示IDR对基因组定位影响有限。然而,PAPA检测显示DBD与全长Sp1之间完全没有可检测的共定位,与CUT&RUN结论直接矛盾。Sp1 IDR-LacI嵌合体在PAPA和共聚焦成像中均与全长Sp1共定位,但CUT&RUN未检测到任何富集峰。进一步实验发现,CUT&RUN透化步骤导致大量Sp1从细胞核流失至上清,而组蛋白H2B则保持稳定,提示透化处理选择性丢失了弱结合的TF分子,使测序方法系统性高估DBD对染色质结合的贡献。
2.6 活体果蝇多线染色体成像证实IDR赋予基因座特异性
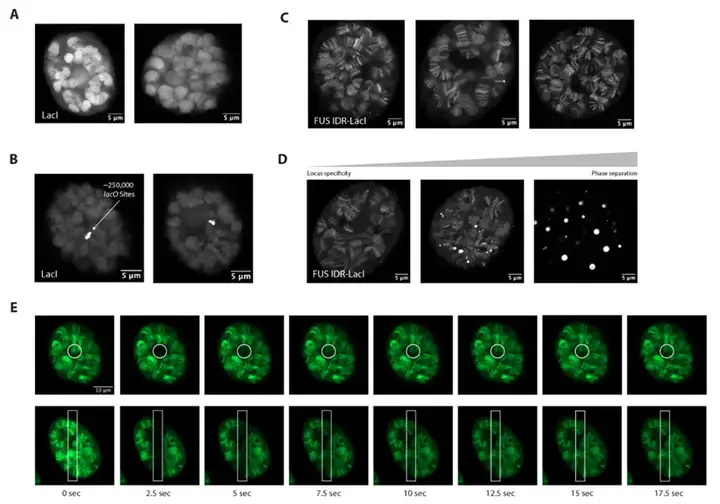
在果蝇唾液腺细胞中,LacI单独表达时在多线染色体上呈均匀非特异性分布;而将人类FUS IDR融合至LacI后,嵌合体在果蝇基因组(不含lacO序列)的常染色质区域形成离散的染色质条带,表明IDR可赋予非特异性DBD明确的基因座特异性。FRAP实验显示条带内荧光在数秒内迅速恢复,说明这种富集来自瞬时相互作用而非稳定结合。在高表达水平下,FUS IDR-LacI形成球形液滴,条带信号随之消失,提示相分离与基因座特异性结合相互排斥。
总结:
研究者基于实验结果提出涌现特异性框架:真核TF的基因组定位并非由DBD或IDR单独决定,而是在完整核环境中通过多种动态、低亲和力接触集体协同产生,这与依赖折叠结构域稳定配对的经典细菌调控模型存在本质区别。这一框架可解释DBD序列偏好相同的TF占据不同基因组位点、以及TF结合于缺乏可识别基序位点等长期悖论,并提示IDR在真核进化中的扩张与多样化可能正是特异性决定因素从顺式调控序列向反式无序区域转移的结果。在疾病层面,EWS-FLI1等TF融合癌蛋白及Sp1、Klf1等显性DBD突变体,可能通过改变无序相互作用网络而非单纯改变序列特异性发挥致病作用,这一轴线在既往研究中长期被低估。研究者同时坦承,PAPA与SMT无法解析基因组坐标,IDR介导的TF定位是否直接驱动转录激活尚未证明,约1600种人类TF之间的无序相互作用网络仍有待系统探索。



