Mol Cell | 薛愿超团队最新成果:circRNA-RNA互作全景图谱,揭示P-body介导的翻译抑制机制
环形RNA(circRNA)是一类主要通过前体mRNA反向剪接形成的共价闭合RNA分子。尽管近年来研究发现circRNA在组织发育、癌症及免疫调节中发挥重要作用,且部分高表达的circRNA(如CDR1as)在进化上高度保守,但学术界对其靶标全景(target repertoire)及作用机制的理解仍相对匮乏。目前的主流观点主要集中在circRNA作为miRNA海绵或RNA结合蛋白(RBP)的支架功能上,而关于circRNA是否能通过直接碱基互补配对广泛调控其他RNA的研究受到技术限制,以往的方法分辨率低且难以精确定位结合位点。
此外,细胞内的无膜细胞器在RNA代谢中扮演关键角色。虽然已知circRNA在脑组织中高度富集且十分稳定,但它们是否参与以及如何参与无膜细胞器内的RNA互作网络尚不清楚。因此,circRNA是否能通过直接碱基配对与其他RNA互作?这种互作是否与其亚细胞定位通过协同机制调控基因表达?
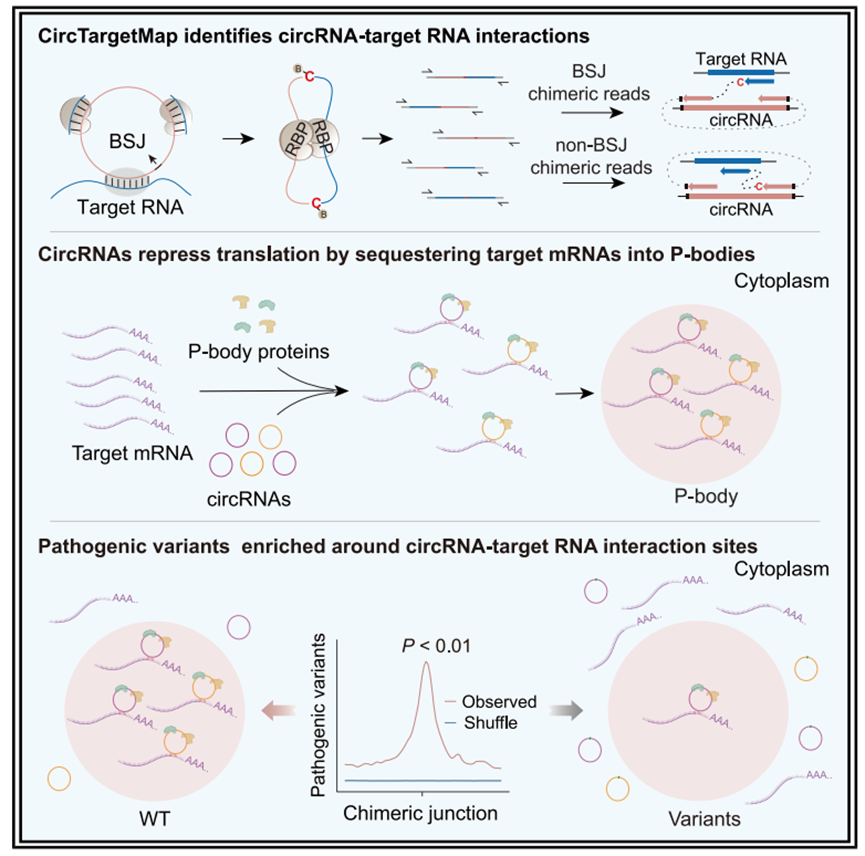
2026年02月16日,中国科学院生物物理研究所薛愿超研究员团队在《Molecular Cell》上发表了题为“Global mapping of circRNA-target RNA interactions reveal P-body-mediated translational repression”的重要研究。该研究开发了一套全新的计算分析流程circTargetMap,利用RIC-seq数据构建了转录组范围内的circRNA-靶标RNA互作图谱。研究团队在多个细胞系和海马组织中鉴定了超过11万个高置信度互作,发现绝大多数靶标mRNA被多个circRNA结合。功能上,研究揭示了CDR1as和circRMST等circRNA通过序列特异性的碱基互补配对,将靶标mRNA隔离至P-body(Processing bodies)中从而抑制其翻译,该过程不依赖于miRNA或AGO2/DICER途径。为进一步验证,团队开发了GRIC-seq技术直接捕获颗粒内的RNA互作,证实了这是一种普遍存在的P-body介导的翻译抑制机制。此外,研究还发现致病性变异显著富集在circRNA与靶标RNA的结合位点,提示该机制在疾病发生中的潜在作用。
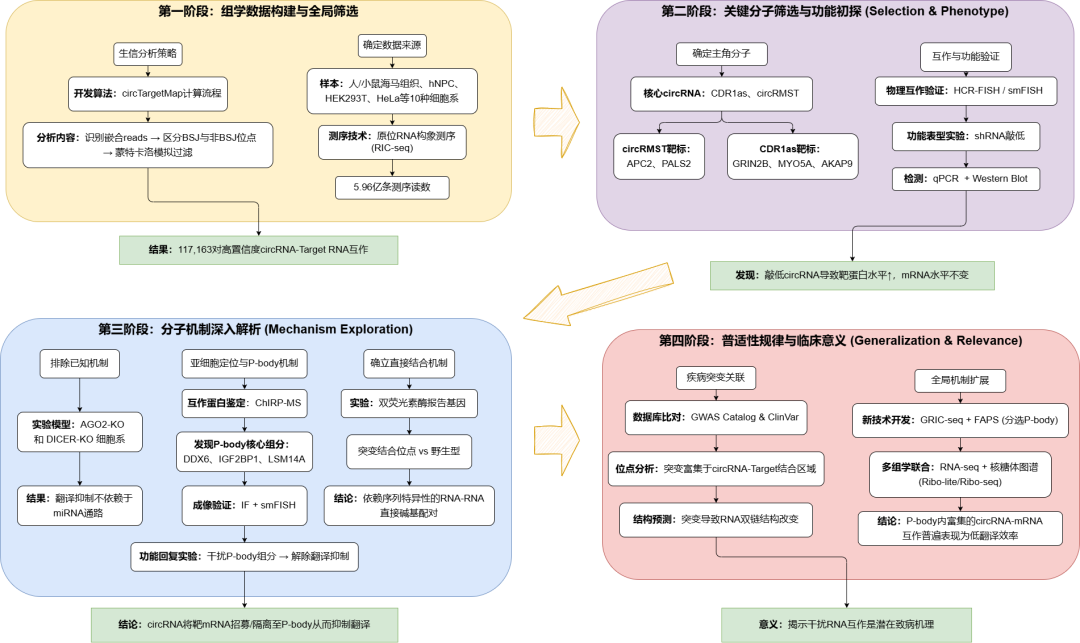
研究技术路线
主要研究结果
1. 全局绘制circRNA-靶标RNA互作图谱
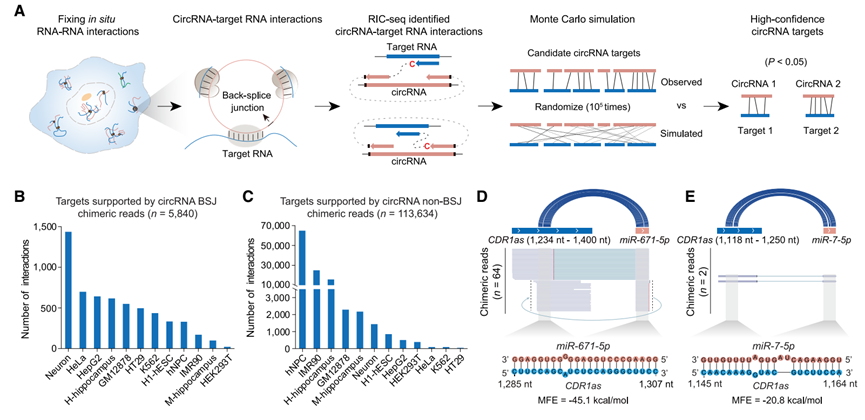
研究团队首先开发了名为circTargetMap的计算分析流程,旨在从RIC-seq数据中系统性鉴定circRNA与其他RNA的相互作用。该策略通过识别跨越circRNA反向剪接位点以及全长序列的嵌合体reads,并结合蒙特卡洛模拟去除背景噪声,成功在10种人类细胞系及海马组织中绘制了高分辨率的互作图谱。分析共鉴定出117,163个高置信度互作,发现绝大多数靶标mRNA被多个circRNA结合,揭示了circRNA广泛的靶向能力。此外,该方法精准重现了CDR1as与miR-7及miR-671的已知互作,验证了策略的可靠性。
2. circRNA在转录后水平抑制靶标mRNA的翻译效率
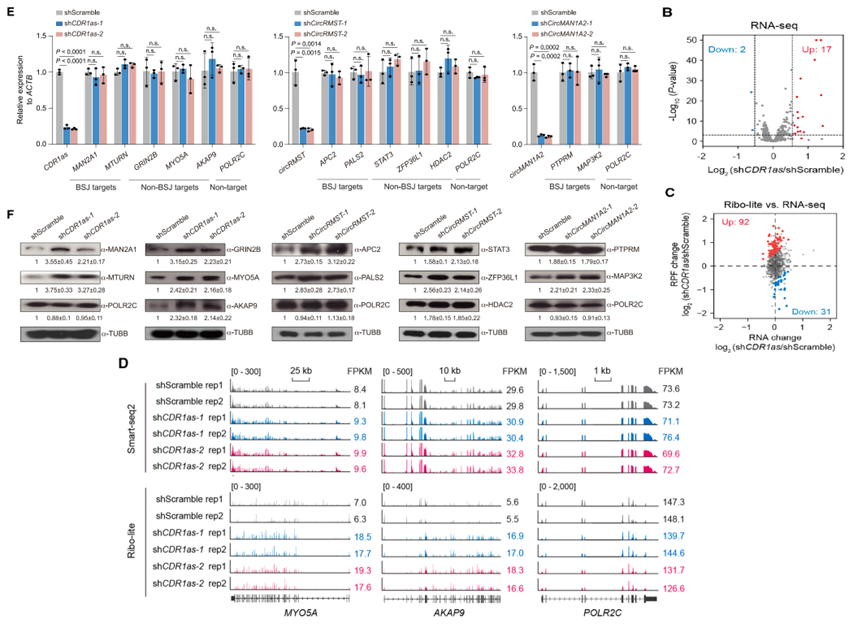
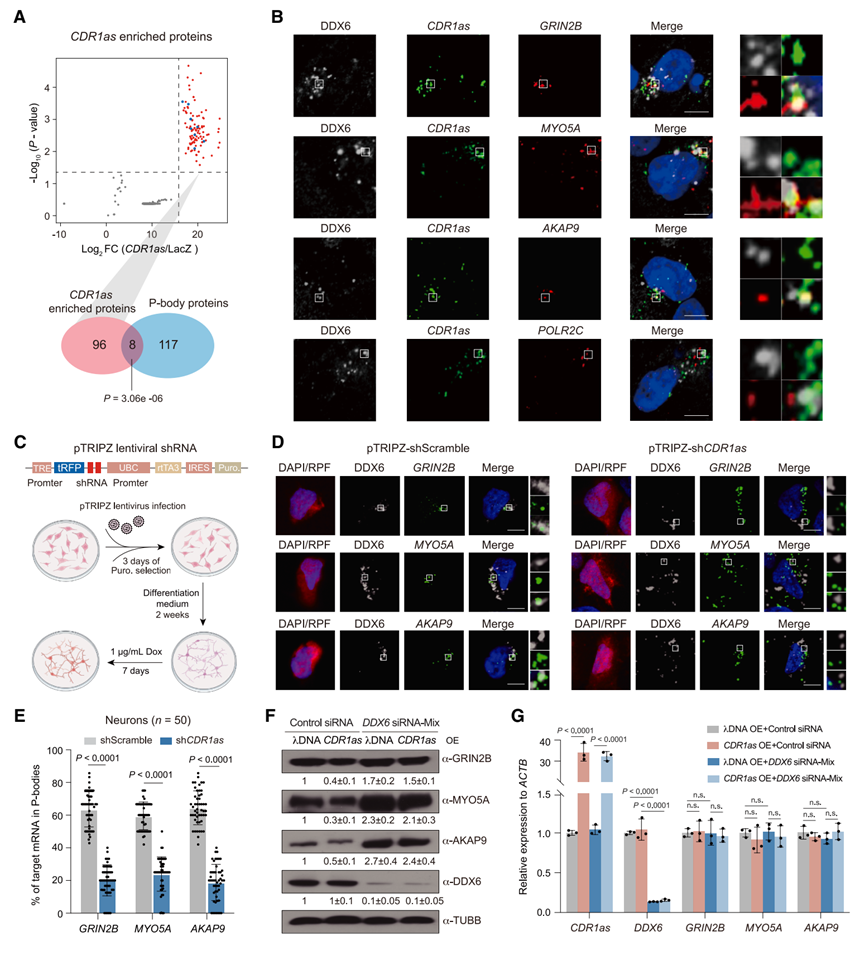
为探究circRNA对靶标RNA的调控功能,研究结合了shRNA敲低、RNA-seq和Ribo-seq(核糖体印迹测序)技术。结果显示,在hNPC来源的神经元中敲低CDR1as、circRMST或circMAN1A2后,其靶标mRNA的转录水平未发生显著变化,但靶标蛋白水平显著上升。全基因组分析进一步证实,CDR1as敲低导致其靶标基因的翻译效率特异性增加,而mRNA丰度保持稳定,表明circRNA主要通过抑制翻译而非促进降解来调控靶标基因表达。
3. 翻译抑制依赖于序列特异性碱基配对与环状拓扑结构
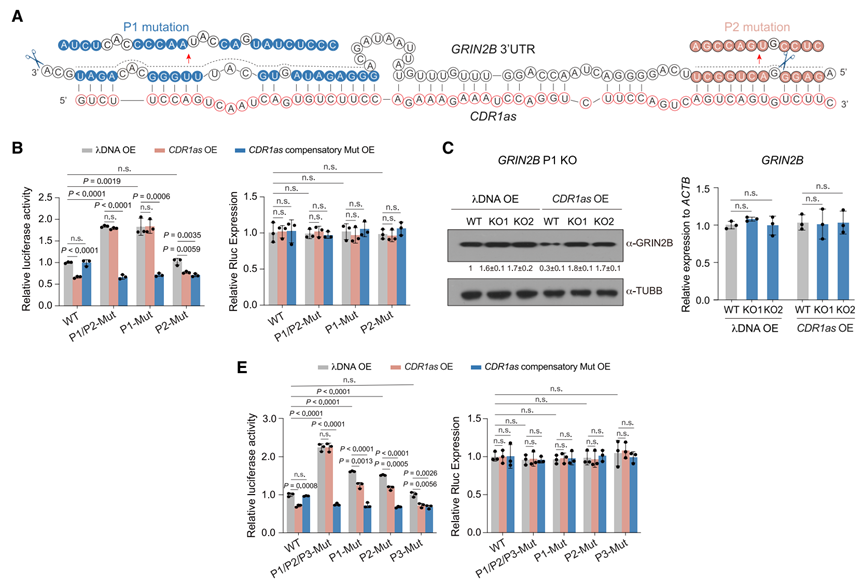
机制研究表明,circRNA对翻译的抑制作用是直接且特异的。通过双荧光素酶报告系统和CRISPR-Cas9基因编辑,研究证实circRNA与靶标mRNA之间的直接碱基互补配对是抑制翻译的必要条件。破坏结合位点会解除抑制,而引入补偿性突变恢复配对则能重新建立抑制。此外,在AGO2或DICER敲除细胞中该抑制作用依然存在,排除了miRNA途径的参与。而且只有闭合环状的circRNA能发挥此功能,线性同源序列无效,揭示了环状拓扑结构的重要性。
4. circRNA通过招募靶标mRNA进入P-body实现物理隔离
为解析翻译抑制的亚细胞空间机制,研究团队利用ChIRP-MS技术鉴定了CDR1as的结合蛋白,发现其显著富集P-body(加工小体)的核心组分。IF/smFISH(高分辨率成像)显示,CDR1as与靶标mRNA在神经元胞质中与P-body标记物DDX6高度共定位。功能缺失实验表明,敲低CDR1as导致靶标mRNA脱离P-body,而破坏P-body核心蛋白则完全阻断了circRNA介导的翻译抑制。这表明circRNA起到了“分子穿梭机”的作用,将靶标mRNA隔离至P-body中以阻止核糖体装载。
5. GRIC-seq揭示P-body内广泛的circRNA介导调控
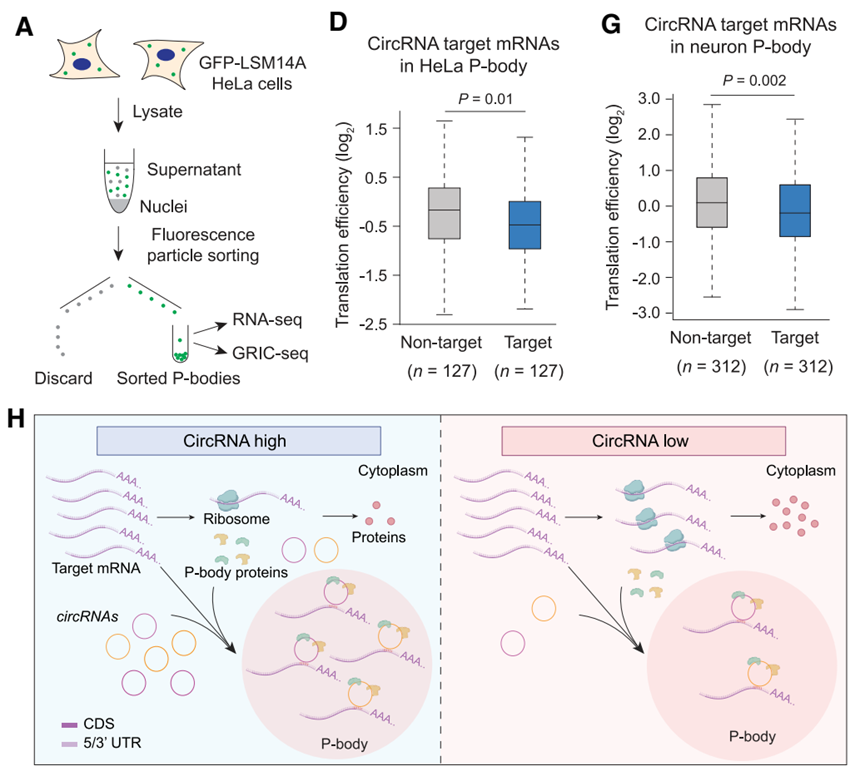
为了直接捕获无膜细胞器内的RNA互作,研究开发了GRIC-seq(Granule RIC-seq)技术。通过FAPS流式分选或免疫沉淀纯化P-body,并在其内部进行原位邻近连接和测序,研究团队绘制了P-body特异性的RNA互作图谱。数据表明,P-body内部富集了数千种circRNA及其靶标mRNA。与非靶标对照相比,这些被circRNA招募至P-body的mRNA在全转录组水平上表现出显著更低的翻译效率,证实了这是一种普遍存在的基因表达调控模式。
6. 致病性变异富集于circRNA结合位点
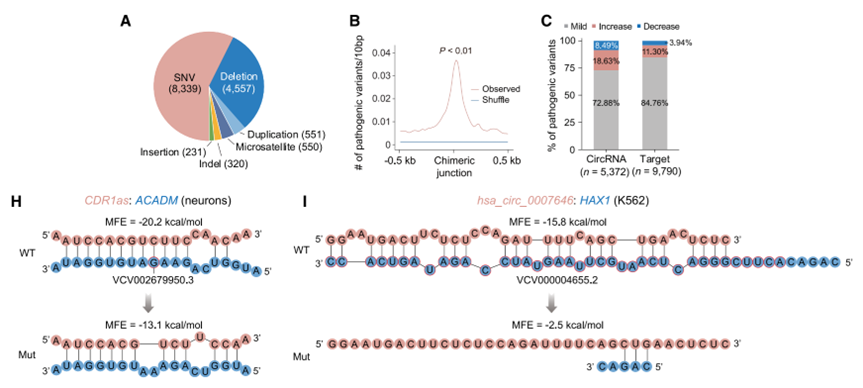
通过将GWAS及ClinVar数据库中的变异位点映射到互作图谱,研究发现致病变异显著富集在circRNA与靶标RNA的结合区域。计算分析表明,约27%的circRNA侧变异和15%的靶标侧变异会显著改变RNA双链的结合能(|ΔMFE|≥ 3 kcal/mol)。例如,ACADM基因上的一个致病性缺失突变削弱了其与CDR1as的结合。这些高影响变异与癌症、神经系统疾病等密切相关,提示破坏circRNA-RNA互作可能是某些遗传疾病的致病机理。
该研究通过开发circTargetMap计算流程和GRIC-seq实验技术,首次在转录组尺度绘制了circRNA与靶标RNA的互作全景图,揭示了circRNA在“miRNA海绵”之外的全新功能模式:即作为分子伴侣通过序列特异性碱基互补配对识别靶标mRNA,并将其招募至P-body这一无膜细胞器中。与线性RNA不同,该机制高度依赖于circRNA的闭合环状拓扑结构,最终导致靶标mRNA在P-body内发生翻译抑制而非降解。该发现不仅解析了P-body作为mRNA储存及翻译抑制中心的分子基础,还阐明了无膜细胞器内RNA互作网络的普遍调控规律。重要的是,研究发现大量破坏这种互作稳定性的致病性遗传变异与神经系统疾病及癌症密切相关,提示circRNA介导的亚细胞定位和翻译调控在维持细胞稳态中起关键作用,为相关疾病的诊疗提供了潜在的RNA干预靶点。