时隔一年曹俊越团队再发Science,解析器官衰老的表观机制
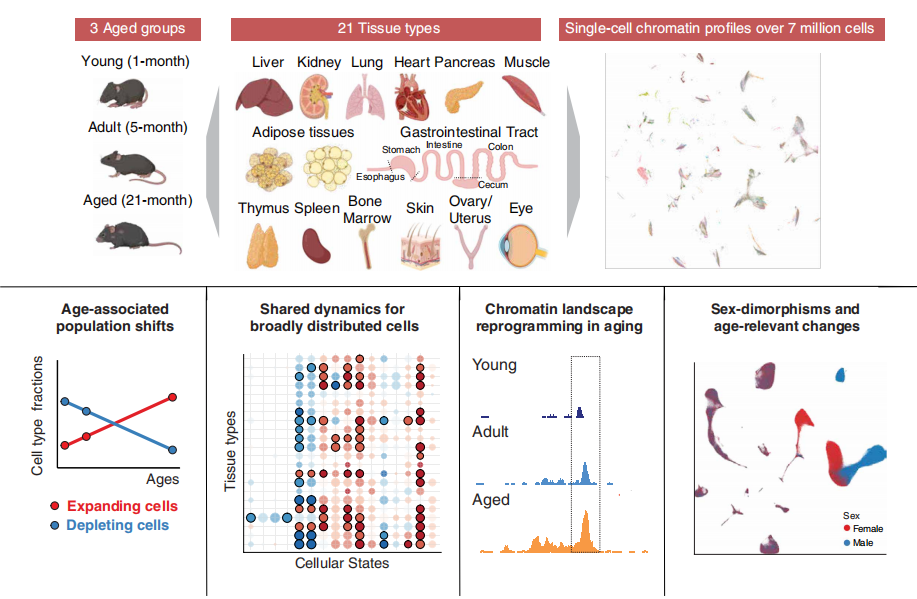
26年2月26日,Science杂志发表题为“Organism-wide cellular dynamics and epigenomic remodeling in mammalian aging”的研究论文。研究团队利用单细胞表观组学技术,系统描绘了小鼠21种组织在三个年龄节点的染色质可及性动态变化,揭示了衰老过程中细胞组成与表观景观的重塑规律,为理解免疫衰老提供了跨组织资源与技术参照。论文通讯作者为洛克菲勒大学单细胞基因组学与种群动力学实验室负责人曹俊越及周伟(zhou wei 音译)。同期, Science杂志配发Sam N. Barnett与Michela Noseda撰写的 Perspective 述评“Chromatin dynamics shape aging across organs”。
值得一提的是,曹俊越教授团队曾于2024年11月28日在 Science杂志在线发表题为“A panoramic view of cell population dynamics in mammalian aging”的论文,利用单细胞转录组技术扫描小鼠五个生命阶段、逾2100万个细胞,系统解析了器官衰老的细胞动态图谱。时隔一年,依然是Science杂志,曹俊越团队这次将研究的主题从解析“谁”变化了(转录组)转向了谁调控了基因转录变化(表观组学,染色质开放性),这一转变也印证了生物医学机制研究的一个底层逻辑:从发现“谁”在变,升级为探索“怎么变”的思路精进。

本文通过构建覆盖21种组织、逾千万核的单细胞染色质可及性图谱,系统揭示了小鼠衰老过程中染色质景观的重塑规律。研究发现衰老伴随特定细胞类型的协同性扩张或消减,并在跨组织水平上观察到免疫重构、功能性细胞类型耗竭及炎症相关状态的涌现。在分子层面,衰老诱导了广泛的染色质重编程,包括顺式调控元件的细胞类型特异性使用变化及转录因子基序可及性改变,这些染色质动态与靶基因表达存在显著关联。值得注意的是,作者发现了显著的性别二态性:相同细胞类型在衰老过程中呈现性别特异的染色质状态维持模式,且细胞组成与分子层面均存在年龄-性别交互效应。该跨器官单细胞表观基因组图谱不仅揭示了衰老重塑细胞组成与调控区域的分子逻辑,还为评估抗衰老干预措施、理解染色质动态与组织生理学交叉机制提供了关键参考。作者提供了一个在线资源平台:https://epiage.net/
主要科学问题与研究意义
染色质可及性是基因表达调控的关键环节。衰老相关转录组的变化已有多项报道,但染色质可及性相关的研究数据还不很完善,且缺乏全组织范围的系统性研究。本文提出了通过单细胞表观组学技术绘制全组织染色质可及性图谱,以揭示衰老过程中的染色质重塑。基于这一考虑,文章提出了以下核心科学问题:衰老过程中,全组织范围内的细胞组成和染色质可及性如何变化?这些变化是否具有组织特异性?是否存在跨组织的共同变化模式?染色质重塑与基因表达变化之间如何关联?性别是否在衰老相关的细胞和染色质变化中发挥作用?
本文的主要工作和意义可以概括为:
构建全组织单细胞染色质可及性图谱:文章首次构建了涵盖21种组织类型、跨越三个年龄阶段(1个月、5个月、21个月)和两种性别的全组织单细胞染色质可及性图谱。这一图谱为理解衰老过程中的染色质重塑提供了前所未有的资源。
揭示衰老相关的细胞组成变化:通过分析图谱数据,文章揭示了衰老过程中细胞组成的广泛变化,包括免疫细胞和非免疫细胞的动态变化。这些发现有助于理解衰老过程中组织稳态的丧失和功能衰退的机制。
发现跨组织的共同衰老模式:尽管不同组织表现出特定的衰老相关变化,但文章也发现了跨组织的共同衰老模式,如免疫重塑、功能性细胞类型的广泛耗竭和炎症相关状态的出现。这些发现为理解衰老的系统性特征提供了新视角。
解析染色质重塑与基因表达变化的关联:文章通过整合染色质可及性数据和转录组数据,揭示了染色质重塑与基因表达变化之间的紧密关联。这些发现有助于理解衰老过程中基因表达调控的分子机制。
揭示性别在衰老过程中的作用:文章发现衰老相关的细胞和染色质变化存在显著的性别差异。这一发现强调了性别在衰老研究中的重要性,并为开发性别特异性的抗衰老策略提供了依据。
提供抗衰老干预的参考资源:文章创建的交互式网站(https://epiage.net/)为研究者提供了探索这些数据的平台,有助于指导抗衰老干预策略的开发和优化。这一资源对于推动衰老生物学领域的研究具有重要意义。
推动单细胞多组学技术的发展:文章通过优化单细胞ATAC-seq技术(EasySci-ATAC),展示了单细胞多组学技术在解析复杂生物过程(如衰老)中的巨大潜力。这一技术进展为未来的单细胞多组学研究提供了有力工具。
基于EasySci-ATAC实现大规模组织样品染色质可及性检测
文章通过构建小鼠全组织单细胞染色质可及性图谱,系统地揭示了哺乳动物衰老过程中的细胞动态变化和表观基因组重塑特征。研究团队应用优化的单细胞转座酶可及染色质测序技术(EasySci-ATAC),对跨越三个年龄阶段(1月龄、5月龄和21月龄)和两个性别的21种组织、超过1000万个细胞核进行了分析,成功鉴定出130万个顺式调控元件,并定义了536种组织水平主要细胞类型和1828种更精细的亚型。这一数据集不仅为理解衰老过程中的细胞组成变化提供了前所未有的细节,还揭示了广泛存在的染色质可及性重编程现象。
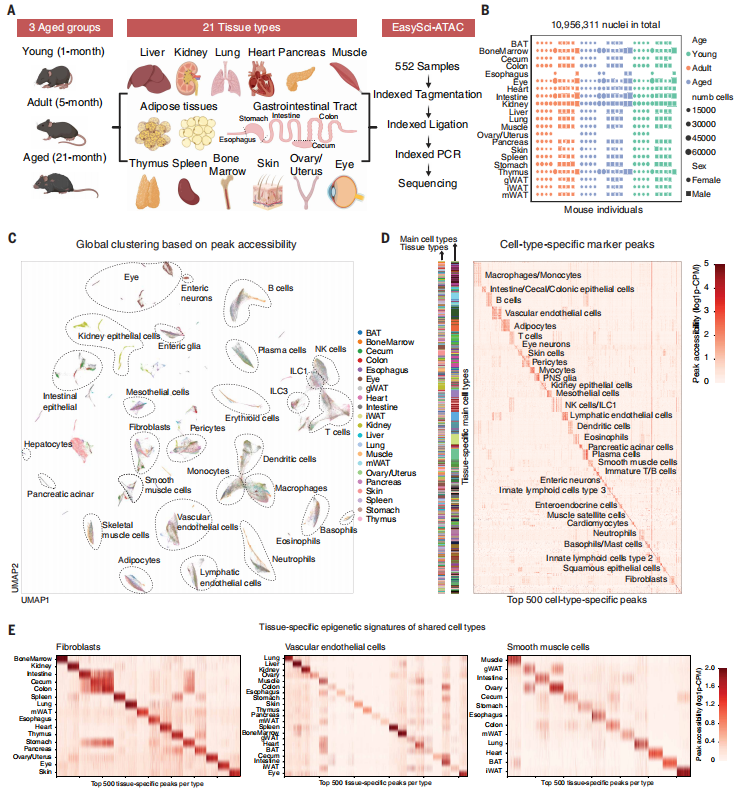 图2 衰老的生物体单细胞染色质可及性图谱 (图片引自[1])
图2 衰老的生物体单细胞染色质可及性图谱 (图片引自[1])
簇水平解析年龄和性别依赖的细胞群体变化
作者观察到不同组织间细胞类型比例的显著差异,其中不乏占比不足1%却功能关键的稀有类群,例如肺部的Ascl1+神经内分泌细胞和晶状体的Gja8+上皮细胞,这恰恰凸显了高通量技术在捕捉这些罕见细胞类型时的重要性。在染色质景观层面,作者发现多数细胞类型在两性间并无差异,但肝细胞、肾近端小管细胞等特定类群却展现出强烈的性别特异性特征,其调控机制与HOX/KLF基序及雄激素响应元件密切相关。进一步分析衰老对细胞群体动态的影响,作者识别出146种丰度随年龄显著变化的器官特异性细胞类型。其中,衰老扩张的细胞中近七成来自免疫谱系,包括广泛扩增的浆细胞、巨噬细胞以及组织特异性扩增的库普弗细胞和γδT细胞;而衰老耗竭的29种细胞类型则多为组织特异性群体,涵盖免疫祖细胞及多种功能性细胞,从卵巢颗粒细胞、皮肤黑素细胞到肾足细胞、肌肉卫星细胞,部分类群在5月龄即出现逾50%的减少,提示衰老效应的早期启动。尤为引人注目的是55种呈现显著年龄-性别交互作用的细胞类型,除多数免疫细胞呈现性别偏向性扩张外,某些细胞甚至表现出相反的动态轨迹,如肾近端小管亚型在雌性中增加却在雄性中减少。通过跨平台验证,作者证实了这些衰老相关细胞动态的保守性和可重复性,为理解器官衰老的细胞逻辑提供了系统性见解。
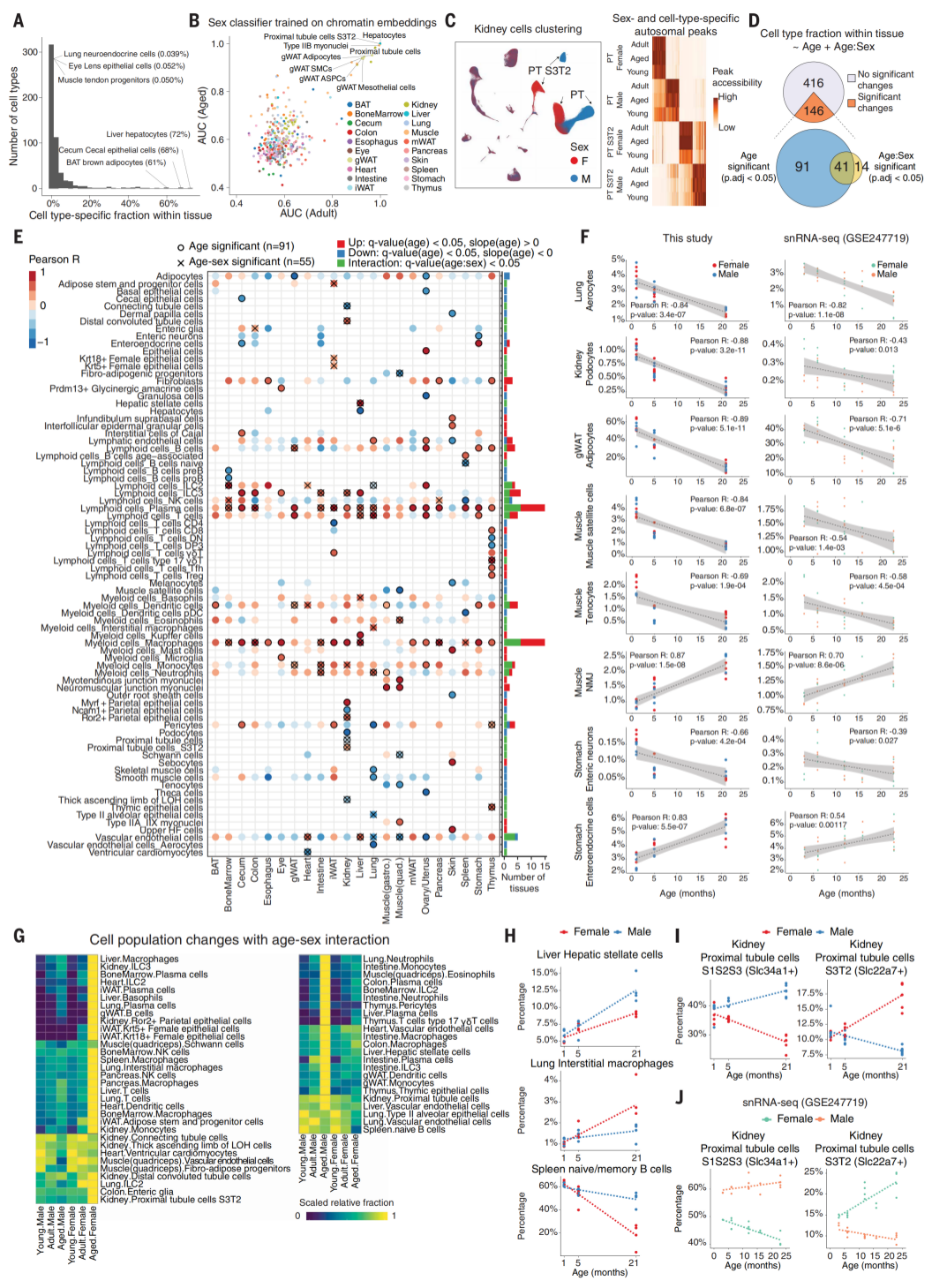 图3 年龄和性别依赖的细胞群在主要细胞类型水平上发生变化 图片引自[1])
图3 年龄和性别依赖的细胞群在主要细胞类型水平上发生变化 图片引自[1])
亚型水平年龄和性别依赖性细胞群体的变化
在细胞亚型层面,衰老的机制远比想象的更为精细和复杂。通过对386种主要细胞类型进行深入再分群,作者识别出1828个具有独特染色质 landscapes 的亚型,其中许多是此前单细胞表观组学研究未能触及的罕见群体,例如肠道中占比不足0.1%的各种内分泌细胞。当作者聚焦于这些精细亚型在衰老过程中的动态时,发现了一些在主要细胞类型层面被掩盖的深刻变化:比如,衰老肠道中特定成纤维细胞和肥大细胞亚群的扩张,以及肝脏与肺部中初始T细胞亚群的耗竭,都与其所属主群体的整体趋势相悖。更引人注目的是,同一细胞类型下的不同亚型甚至会表现出截然相反的衰老轨迹,骨髓中的淋巴偏向性造血干细胞随增龄减少,而巨核细胞偏向性的亚型却在增加。这种异质性还体现在空间上,例如肾脏血管内皮细胞中,仅有位于髓质和静脉的特定亚型发生显著耗损,揭示了同一细胞类型在不同微环境中的“区域脆弱性”。与此同时,作者发现多个在衰老中扩张的亚型,尽管来源不同(如肾小管的不同节段),却共享一套激活的炎症与应激相关转录因子程序,暗示存在跨细胞类型的、协调的衰老响应模式。最后,通过与独立单细胞转录组数据的正交验证,作者确认了这些亚型的生物学真实性及其衰老动态的可靠性,为理解衰老如何精细地重塑细胞生态系统提供了全新的维度。
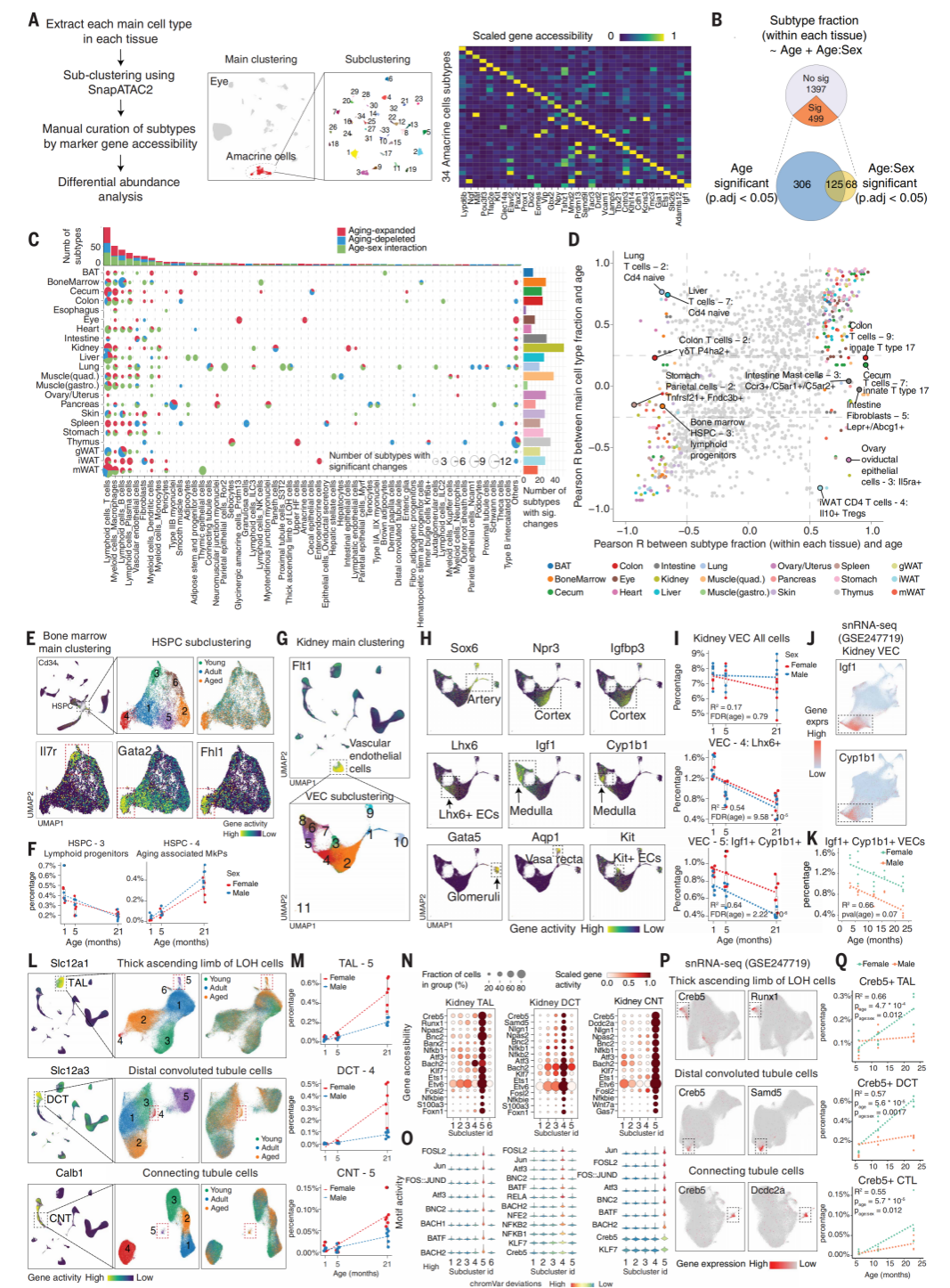
图4 年龄和性别依赖的细胞群在主要细胞类型水平上发生变化 图片引自[1])
广泛分布的免疫细胞亚型与衰老相关的种群动态
广泛分布于全身的免疫细胞和基质细胞在衰老过程中,它们在不同器官里的命运变化是各自为政,还是遵循着某种协同的节律?分析结果显示,答案并非一概而论。免疫细胞呈现出高度协调的跨器官重编程。一方面,作者观察到一种系统性的耗竭:naïve T细胞、前体B细胞和多种组织驻留细胞在多个器官中同步减少。另一方面,则是特定炎症亚群的协同扩张,比如Tbx21+的年龄相关B细胞(ABCs)、表达Ifi211的促炎NK细胞,以及多种效应/调节性T细胞亚型,它们在全身多处组织同时扩增。更有趣的是,这种免疫重塑存在显著的性别二态性。例如,Gzmk+ CD8耗竭T细胞在雌性个体中扩张更为明显,而17型先天性免疫细胞则在雄性中占主导。总体来看,雌性表现出更广泛的免疫活化倾向,这或许为理解人类自身免疫病的性别差异提供了线索。相比之下,血管内皮细胞、成纤维细胞和平滑肌细胞这些非免疫细胞,其命运则高度受限于局部微环境。它们绝大多数表现出强烈的器官特异性,很少出现跨器官的协同变化。例如,肾脏和肺脏的特定内皮细胞亚群在衰老中耗竭,而肝脏和胰腺的某些内皮亚群却显著扩增。不过,在这种特异性之外,作者也发现了个别共享的衰老模式,例如一种Slc7a14+静脉内皮细胞亚群在多种组织中同步减少,揭示了一种普遍存在的血管脆弱性。衰老对细胞命运的重塑是“系统性协调”与“局部微环境决定”两种逻辑共同作用的结果:免疫系统作为整体被重新编程,而实体器官的基质细胞则更多地响应其所在生态位的特异性变化。
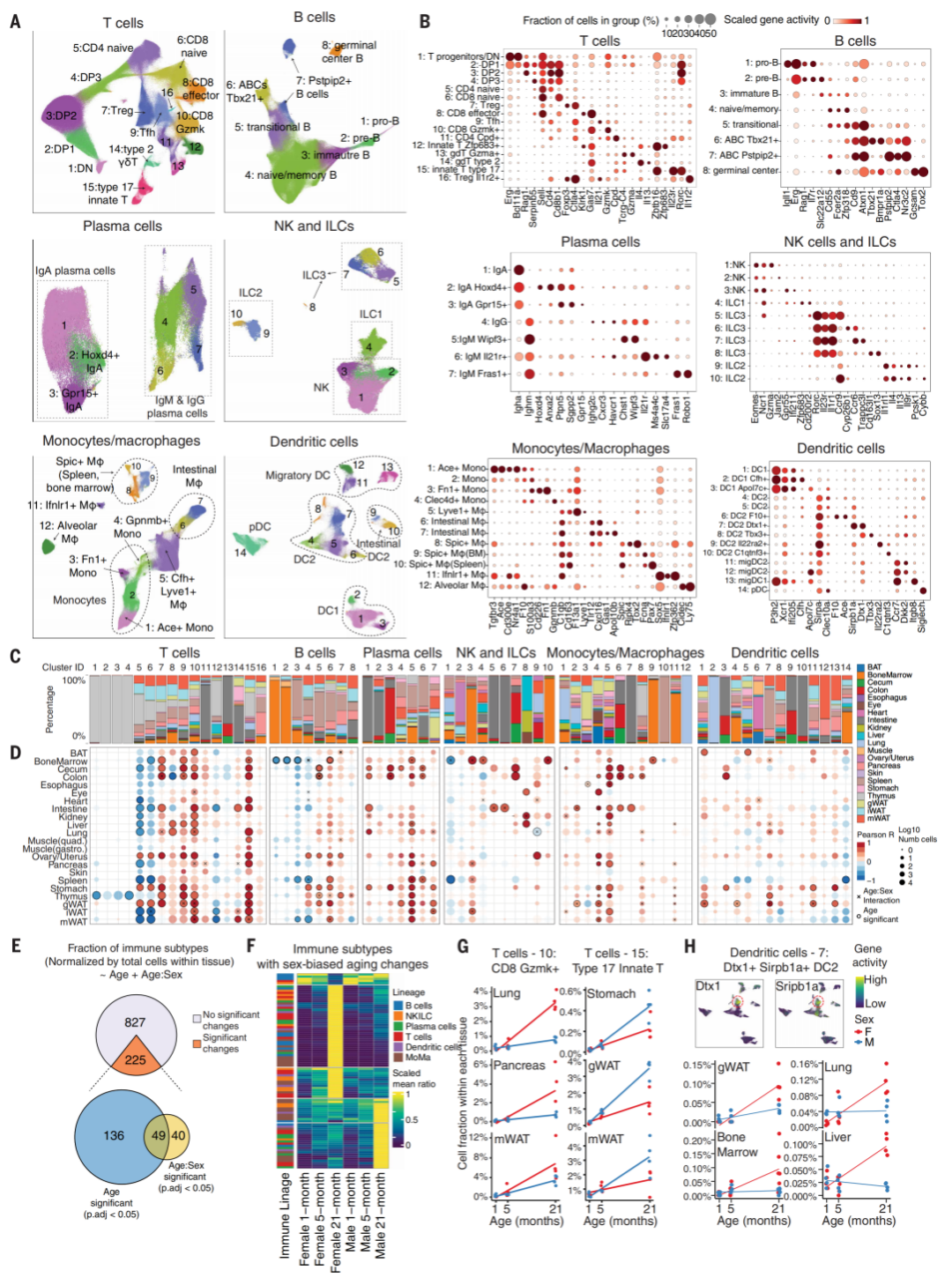 图5 广泛分布的免疫亚型的衰老相关动力学 图片引自[1])
图5 广泛分布的免疫亚型的衰老相关动力学 图片引自[1])
衰老的年龄和性别依赖的表观遗传特征
作者接下来从全器官层面解析了表观遗传的衰老程序,通过对349种器官特异性主细胞类型进行性别分层的差异可及性分析,将差异位点与潜在靶基因关联,并推断了其上游调控因子,包括内源性转录因子和外源性细胞因子信号。结果共鉴定出超过百万个衰老相关的细胞类型特异性差异峰,其中大部分具有细胞类型限制性,但也有803个峰在至少10种细胞类型中呈现一致的衰老变化,提示存在协调性的衰老程序。例如,盐皮质激素受体Nr3c2和前炎症因子Il7的启动子区域在多种免疫细胞中随衰老变得更为开放,而转录因子Sox4和Sox11的启动子可及性则普遍下降,后者在内皮细胞中尤为显著。有趣的是,部分位点的变化方向在不同谱系间截然相反,如Epha3的内含子峰在T细胞和巨噬细胞中上升,却在非免疫细胞中下降,凸显了调控的细胞类型特异性。
从基因组分布来看,衰老上调的差异峰显著富集于LINE和LTR等逆转录转座子元件,提示衰老过程中逆转录元件的去抑制;而衰老下调的差异峰则具有显著更高的保守性评分,表明衰老削弱了进化上保守的发育调控程序。
性别差异同样显著:作者鉴定出近20万雌性特异性和14万雄性特异性的衰老上调位点,涉及衰老相关基因Cdkn2b、干扰素诱导基因Ligp1和Ifi211等。以肝细胞为例,衰老雌性中富集与细胞外基质重塑相关基因Bnc2关联的位点,而衰老雄性则富集脂滴组织基因Cidea相关位点;肾近曲小管细胞中,Mill2相关位点仅在衰老雌性中升高,而Tifa内含子峰仅在衰老雄性中升高,后者恰好对应作者之前观察到的该细胞类型在雄性中的特异性耗竭。这些性别和细胞类型特异性的表观变化与启动子可及性和基因表达变化高度一致。
通过将非启动子差异峰与启动子进行共可及性关联,并整合单细胞转录组衰老图谱,作者构建了超过两万条细胞类型特异的“基因-启动子-增强子”调控链条。以Nr3c2为例,其与25个增强子元件存在关联,这些元件在多种免疫细胞的衰老过程中可及性同步升高,与其启动子活性和基因表达变化高度一致,共同勾勒出这一核心调控因子在免疫衰老中的潜在作用。
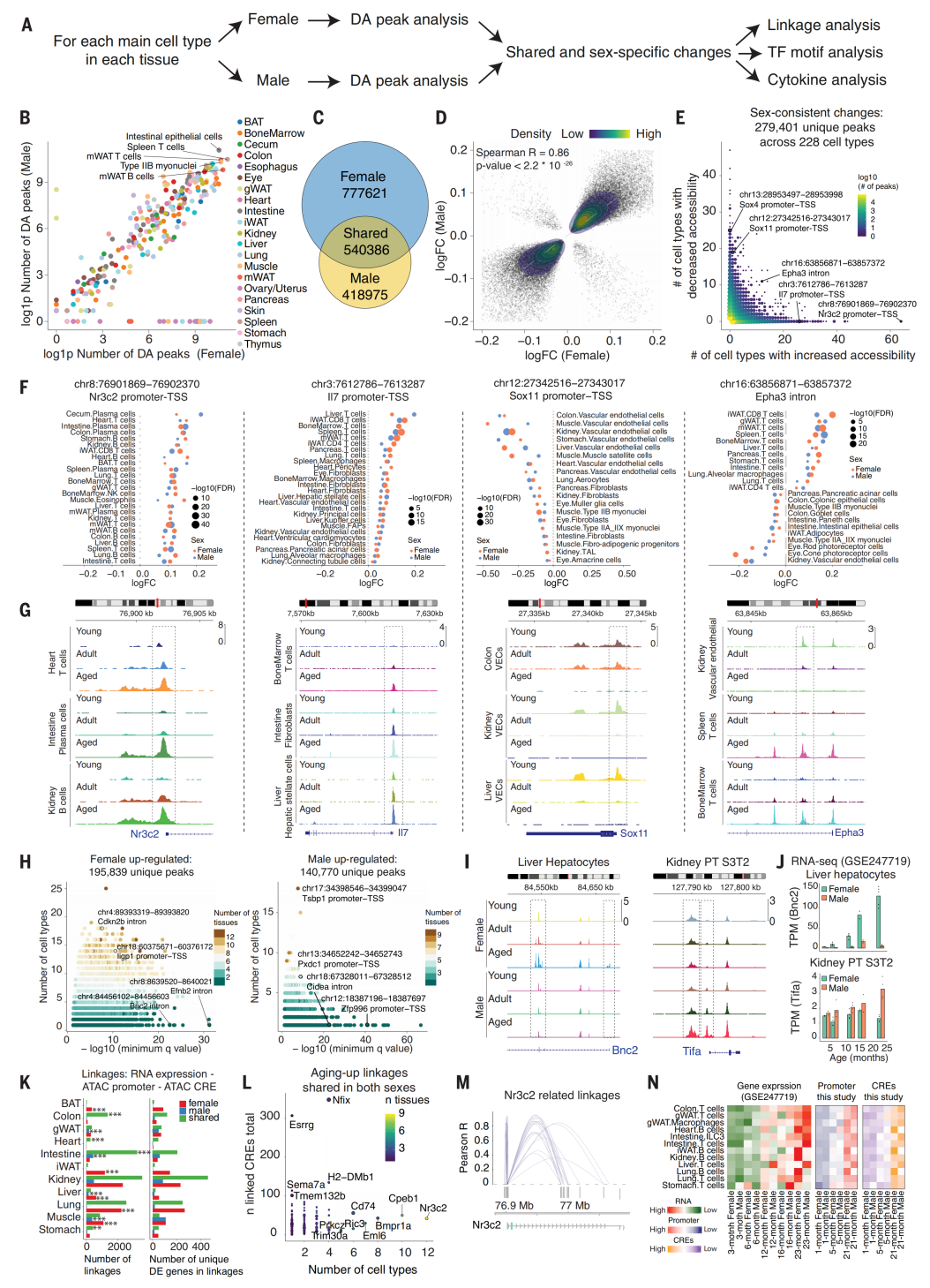
图6 衰老相关染色质可及性变化 图片引自[1])
哺乳动物衰老表观遗传重编程的内在和外在调节因子
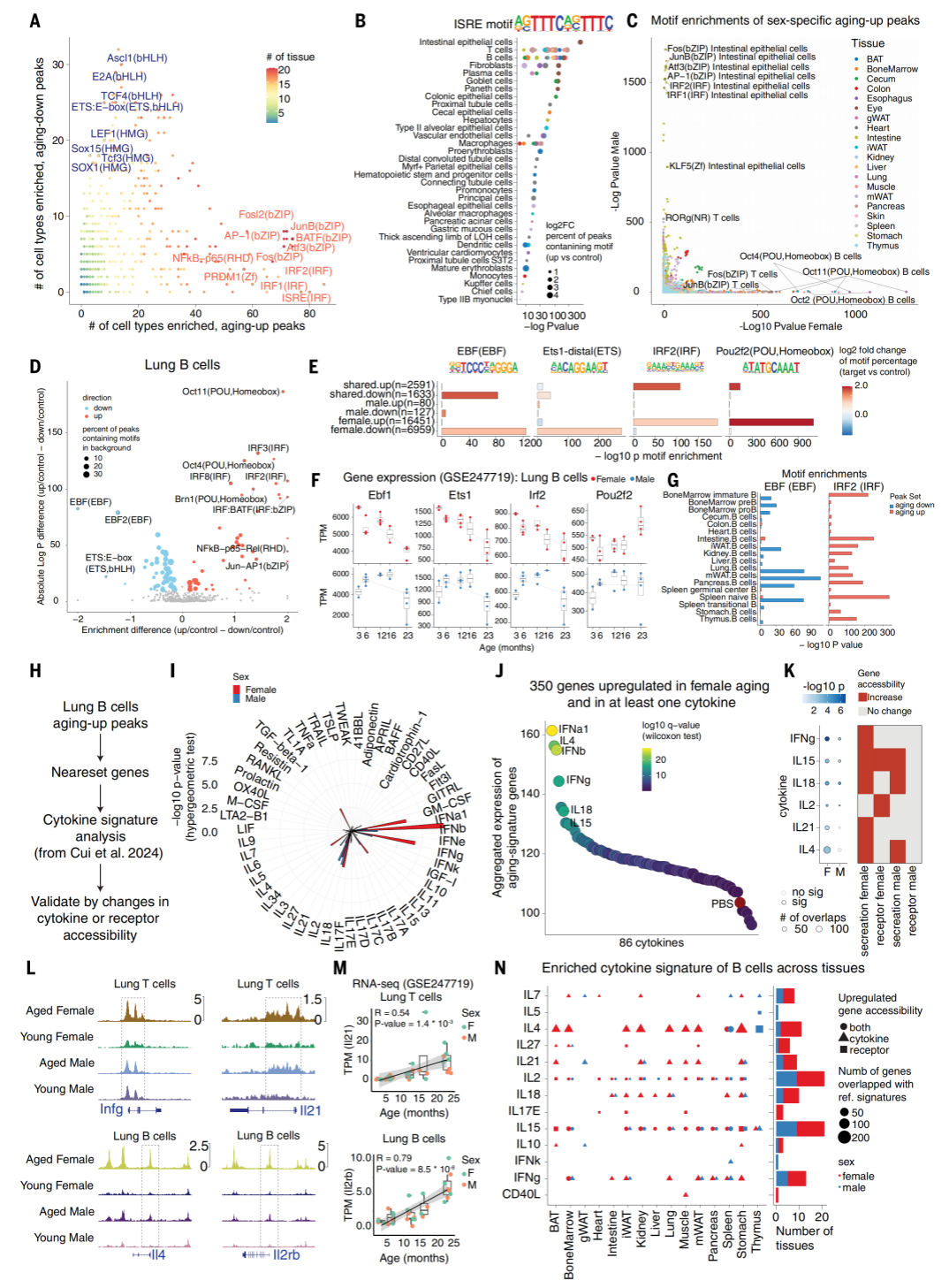
为了探究衰老相关染色质变化的上游调控因子,作者对各细胞类型中差异可及性区域进行了转录因子motif富集分析。结果非常清晰:在超过70种细胞类型中,衰老上调的区域显著富集于炎症相关的motif,比如干扰素刺激反应元件和AP-1;而衰老下调的区域则主要富集于干细胞维持相关的转录因子家族,例如SOX15。性别特异性也很明显,比如雌性B细胞中上调区域富集了POU motif,而雄性肠道上皮细胞中则主要富集炎症转录因子motif。
有趣的是,这些转录因子活性的变化与基因表达数据高度吻合。以肺部的衰老B细胞为例,B细胞发育和静息维持的关键因子Ebf1和Ets1的motif可及性降低,其表达也随之下降;相反,作为炎症信号转录抑制因子的Irf2,其motif可及性增加。更重要的是,早期B细胞因子和干扰素调控因子家族的这种变化在多个组织的B细胞中普遍存在,提示衰老过程中B细胞经历了一个全局性的染色质状态转变。进一步分析发现,大约四分之一的转录因子,其motif可及性的变化与它们所调控的靶基因表达变化方向一致,这有力地支持了表观重塑与转录重编程在衰老过程中的紧密偶联。
作者还观察到,衰老的表观调控并非单个转录因子独立作用的结果。通过分析转录因子间的协作,作者发现大量衰老相关的转录因子对,其中一些复合motif的变化比单个因子更为显著,暗示协同调控的重要性。鉴于如此突出的炎症信号,作者很自然地想知道,究竟是哪些细胞因子驱动了这一表观重塑。通过与免疫图谱数据集的比对,作者发现衰老的表观特征,尤其是雌性肺部B细胞的特征,与干扰素、IL4和IL21等特定细胞因子诱导的谱图高度相似。染色质层面的证据也支持这一点:T细胞中Ifng和Il21的调控区域开放度增加,B细胞中Il4和Il15以及相应受体Il2rb的开放度也增加,这些都与上述细胞因子信号的激活相呼应。
作者还发现,B细胞中细胞因子程序的激活是广泛存在的。例如,IL21信号的增强与IL21阳性T细胞的系统性扩增并行,并且在小鼠和人类的血浆蛋白水平上也得到了验证。联系到IL21在自身免疫病中驱动B细胞分化的已知作用,作者推测它在衰老相关的B细胞表观重塑中可能扮演着类似角色。总的来说,这些发现描绘了一幅由炎症信号和细胞因子驱动、受性别因素调控的系统性表观重编程图景。
EasySci-ATAC技术相对于传统技术的优势分析
EasySci-ATAC是在单细胞ATAC-seq基础上通过组合索引策略优化衍生的技术方法。其核心原理基于转座酶Tn5在开放染色质区域的特异性插入能力:Tn5能够识别并切割转录因子结合位点等调控区域,从而标记染色质的可及性位点。为实现单细胞分辨率下的高通量分析,该技术采用了两轮条形码标记策略:在细胞核提取后,首先使用携带不同条形码的Tn5转座酶对细胞核进行第一轮标记;随后在PCR扩增过程中引入第二套条形码对DNA片段进行第二轮标记。通过这种组合索引策略,每个DNA片段最终携带两套独特的条形码信息,从而确保单细胞水平的识别特异性。标记后的细胞核经流式分选、PCR扩增、文库构建及高通量测序,最终通过生物信息学工具进行数据处理、细胞类型识别和染色质可及性分析。
EasySci-ATAC相较于传统Bulk ATAC-seq在多组织样品分析中展现出多维度优势。首先是分辨率维度。传统方法只能提供细胞群体的平均信号,而EasySci-ATAC能够在单细胞水平解析染色质可及性,揭示复杂组织中细胞类型和状态的异质性。其次是通量维度,优化的组合索引策略实现了对大量细胞的同时分析,显著提高了实验效率并降低了成本,使得同时处理来自不同组织的多个样品成为可能。第三是组织适应性维度,该技术通过优化核提取和文库构建方法,适用于多种组织类型,包括传统上难以处理的样本,为跨组织比较研究奠定了基础。
EasySci-ATAC技术的应用为单细胞表观组学领域开辟了新的研究维度。在机制解析层面,该技术能够全面分析组织中的细胞类型动态、细胞状态转变以及新细胞亚群的识别,其数据可与单细胞转录组数据整合,揭示染色质可及性与基因表达之间的调控关联,为理解基因调控网络在生理和病理过程中的变化提供全景视角。在生物标志物与治疗靶点发现层面,通过识别疾病或衰老相关的染色质可及性区域和转录因子结合位点,该技术为发现新型生物标志物和干预靶点提供了分子层面的线索。在跨器官整合研究层面,该技术使得全生物体范围的细胞动态变化分析成为可能,能够揭示不同组织间共享或特异的调控模式,为系统性理解复杂生物学过程提供了关键技术支撑和数据资源。
参考文献
1. Ziyu Lu et al., Organism-wide cellular dynamics and epigenomic remodeling in mammalian aging.Science391,eadw6273(2026).DOI:10.1126/science.adw6273