83%肿瘤清除,11个月无复发:《Nature》重磅!合成超级增强子实现精准免疫治疗
胶质母细胞瘤因其高度异质性和弥漫性生长特征,一直是神经外科领域极难根除的顽疾。近日,爱丁堡大学Steven M. Pollard团队在《Nature》发表研究“Synthetic super-enhancers enable precision viral immunotherapy”,利用人工设计的合成超级增强子(Synthetic super-enhancers,SSE),构建了一套能够识别肿瘤细胞内部转录网络的精密开关。研究人员通过高通量筛选,从数千个候选序列中鉴定出只在肿瘤干细胞内高度激活、而在健康神经细胞中保持静默的调控元件,为实现零伤亡的精准打击奠定了基础。

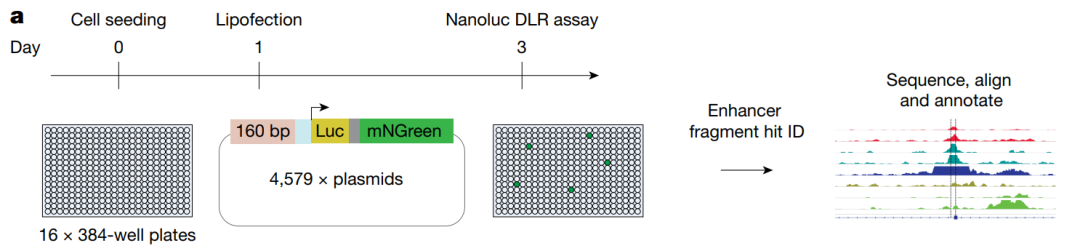
图1. 候选增强子的高通量筛选流程
研究通过ChIP-seq发现高效SSE显著富集了SOX2与SOX9转录因子的结合位点。这两种因子在肿瘤细胞的干性维持中起核心作用,它们以二聚体形式共同锁定SSE序列,产生强力的转录爆发力。研究团队进一步优化的SSE-7元件表现出极高的状态敏感性,一旦癌细胞向成熟神经组织分化,该系统的活性便会迅速下降,从而确保治疗指令仅在具有高增殖潜力的肿瘤群体中执行。
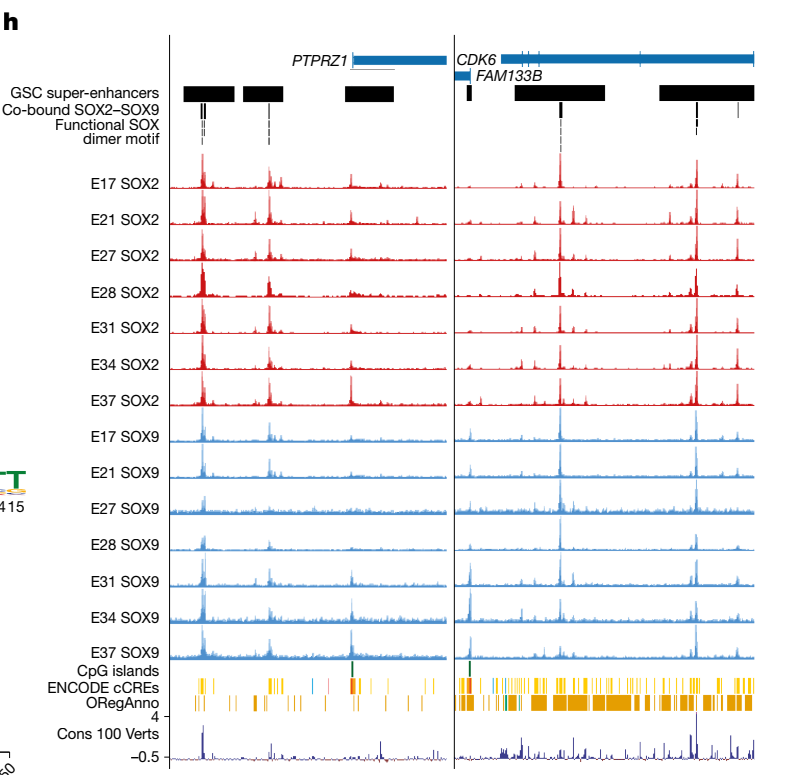
图2. SOX2与SOX9在肿瘤细胞中的协同结合模式
在治疗实施阶段,团队利用腺相关病毒作为载体,将SSE-7驱动的复合指令送入病灶。该指令包含两种核心执行单元:一是诱导肿瘤细胞产生毒性自杀效应的单纯疱疹病毒胸苷激酶即HSV-TK;二是能够招募并激活全身免疫系统防御的白细胞素-12即IL-12。这种双重机制不仅实现了对感染细胞的直接杀伤,还通过改变肿瘤微环境,唤醒了机体针对残余癌细胞的持续免疫排斥反应。
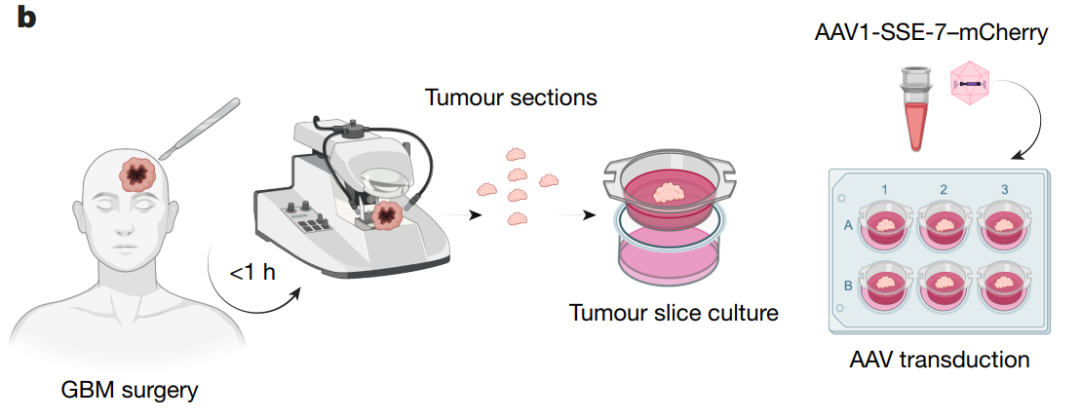
图3. 基于AAV病毒载体的双系统治疗原理示意图
动物实验结果显示,单次局部注射治疗后,约83%(20/24)的实验组小鼠实现了肿瘤的完全清除,且在长达11个月的观察期内未见复发。更具价值的是,康复后的小鼠获得了持久的免疫记忆,能有效排斥再次植入的同类肿瘤。安全性评估证实,SSE-7的表达严格限制在肿瘤区域,未对正常脑组织和系统循环产生副作用。这一成果不仅颠覆了脑瘤的治疗模式,也为基因疗法的精密化调控提供了全新的逻辑框架。
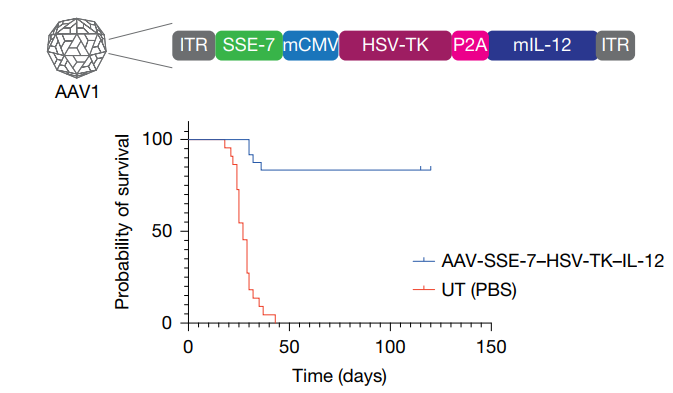
图4. 接受精准基因疗法后小鼠的生存率对比曲线
参考文献:
Koeber U, Matjusaitis M, Alfazema N, et al. Synthetic super-enhancers enable precision viral immunotherapy. Nature. Published online April 8, 2026. doi:10.1038/s41586-026-10329-6