个性化肿瘤mRNA疫苗开发方案:从肿瘤新抗原预测到mRNA疫苗制备
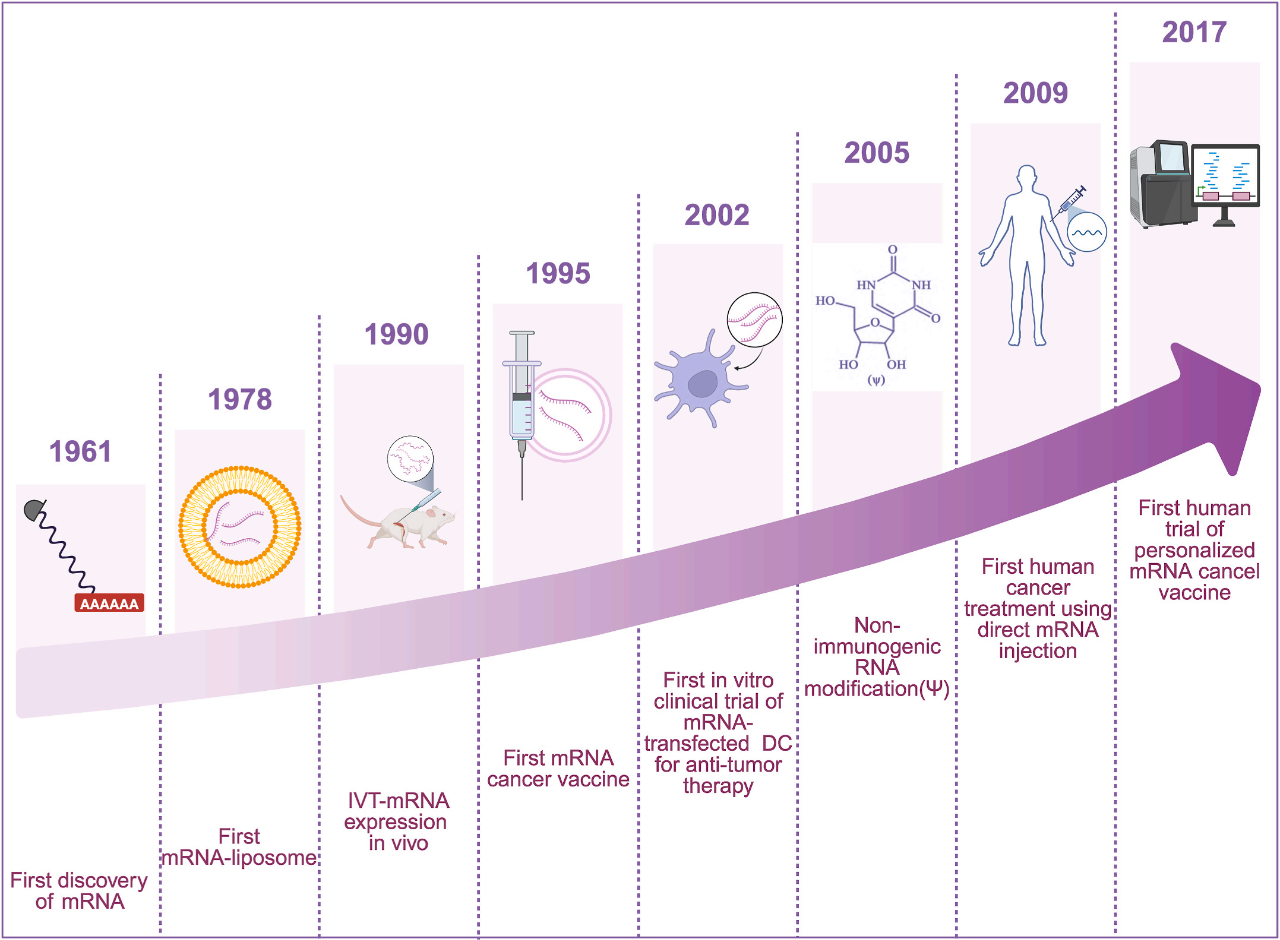
肿瘤mRNA疫苗
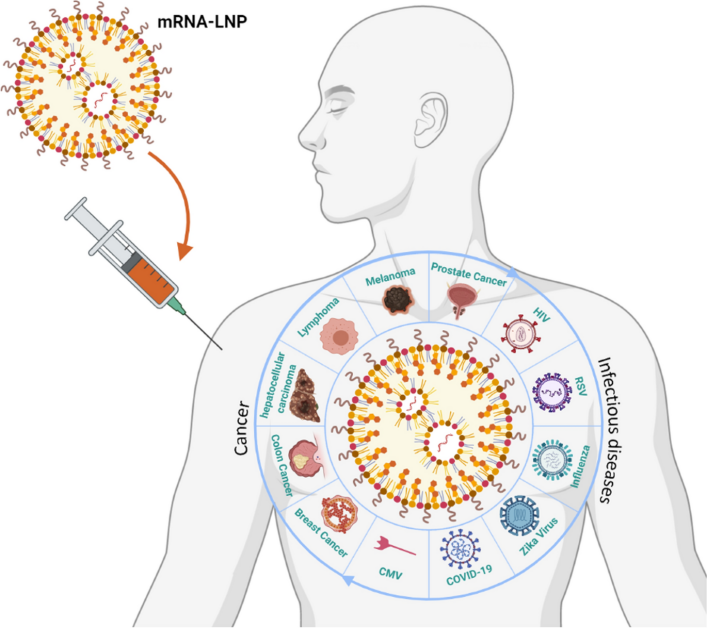
肿瘤新抗原
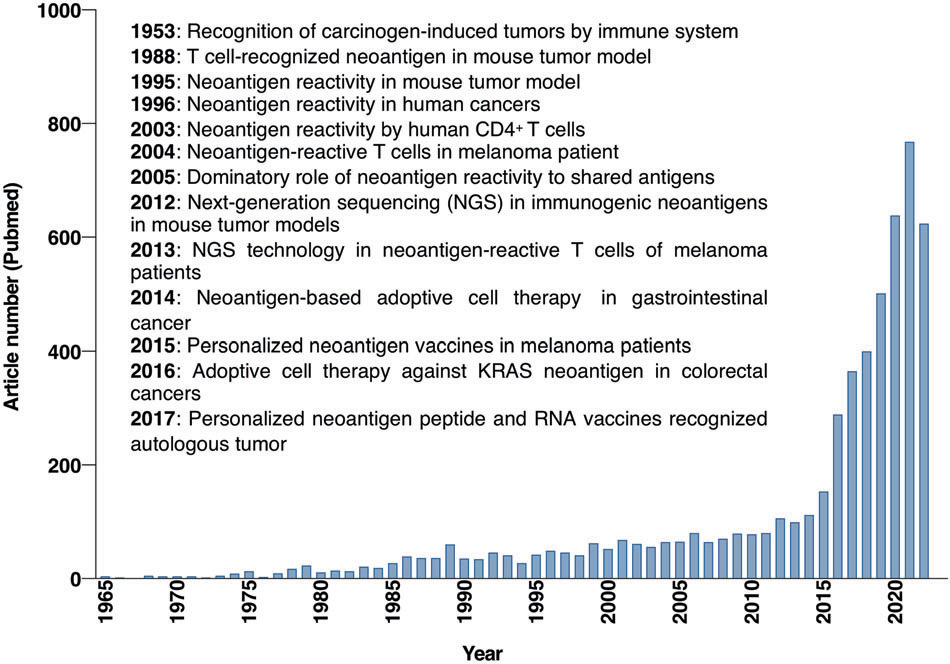
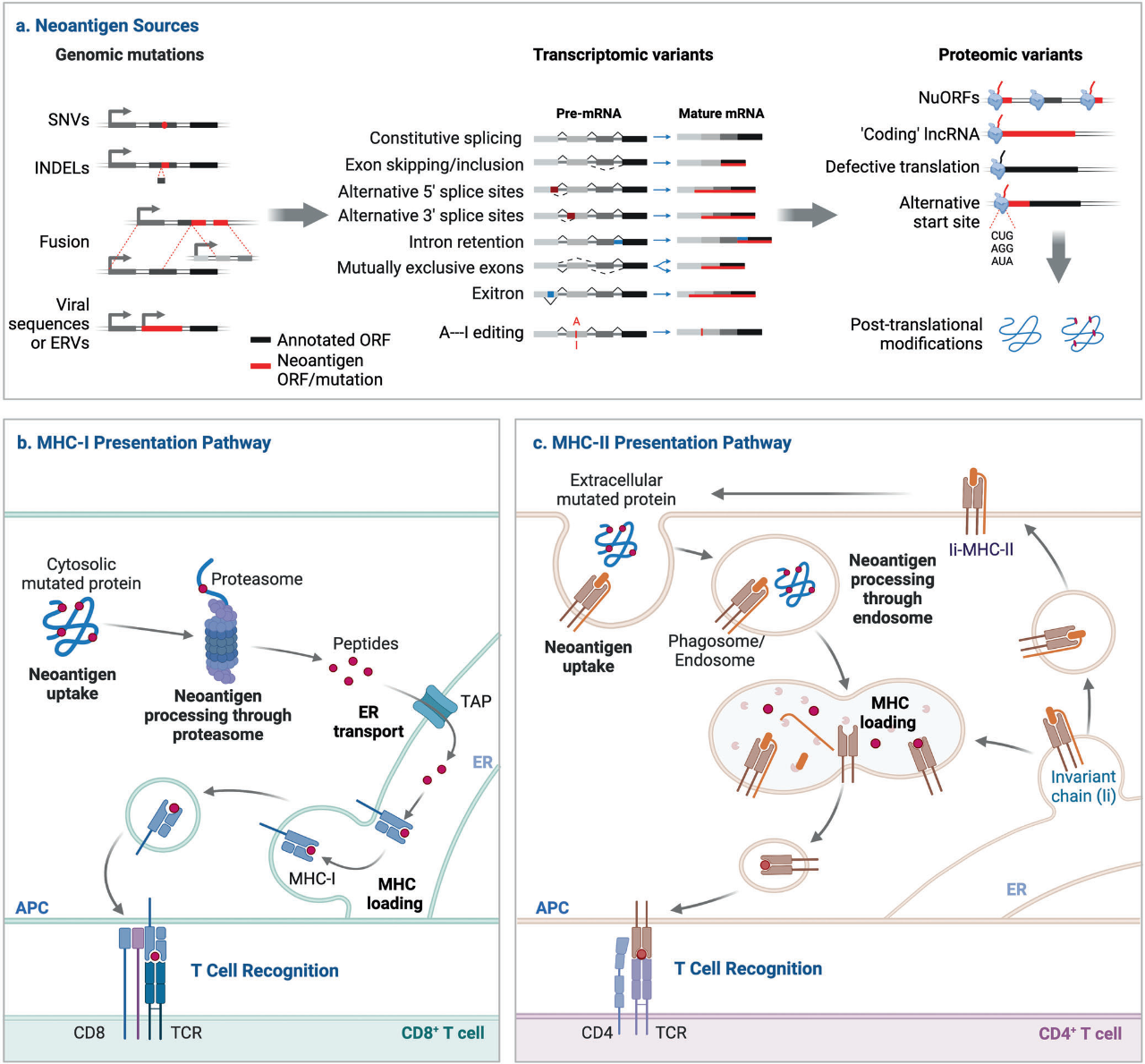
-
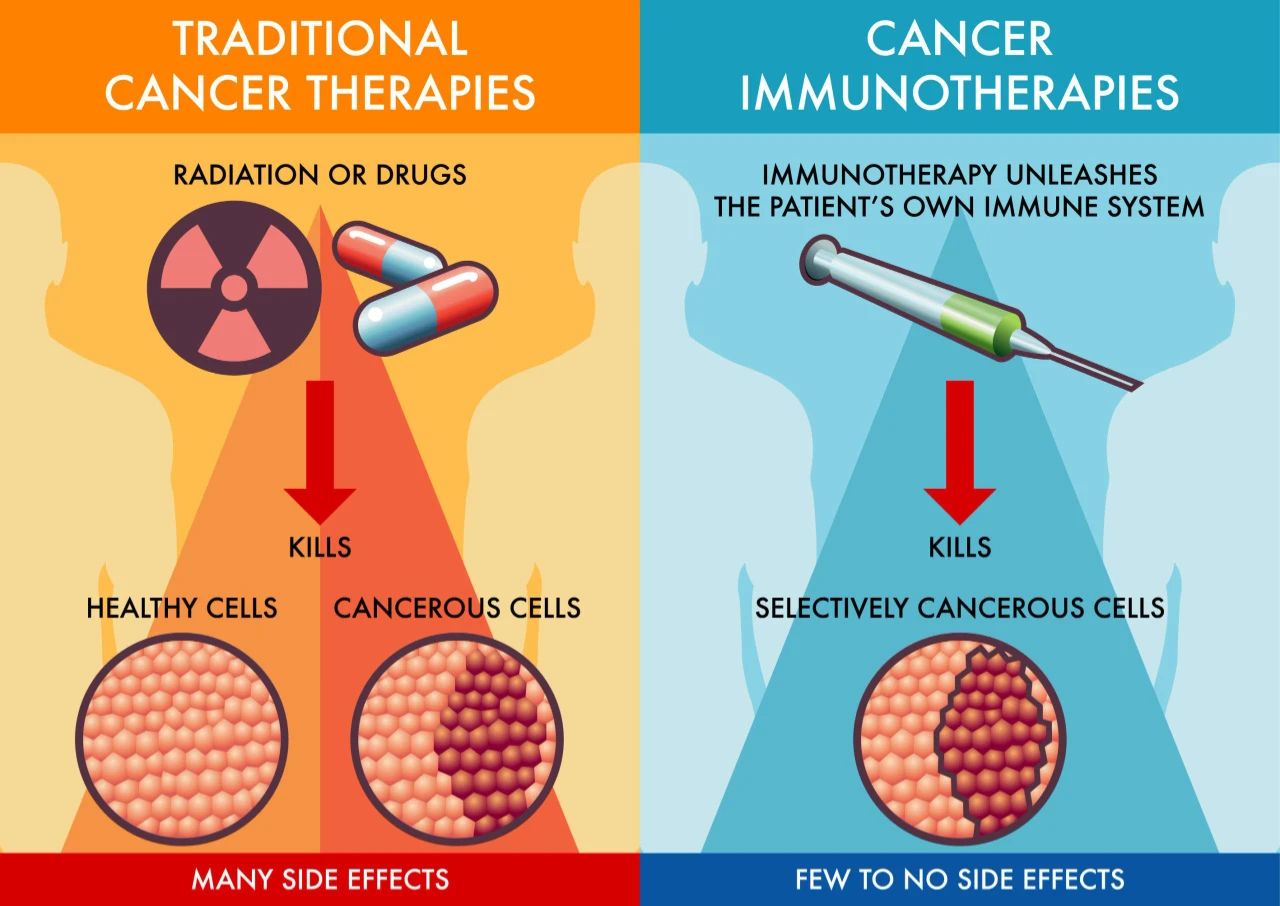
精准靶向肿瘤细胞:新抗原源于肿瘤特有突变,仅表达在癌细胞表面,显著降低对正常组织的脱靶毒性风险。 -
激活双重免疫应答:mRNA疫苗递送的新抗原可同时诱导CD8⁺和CD4⁺ T细胞活化,产生强效且持久的抗肿瘤免疫。 -
高度个体化设计:基于患者特异性突变谱定制新抗原组合,克服肿瘤异质性并兼容PD-1等联合疗法提升疗效。
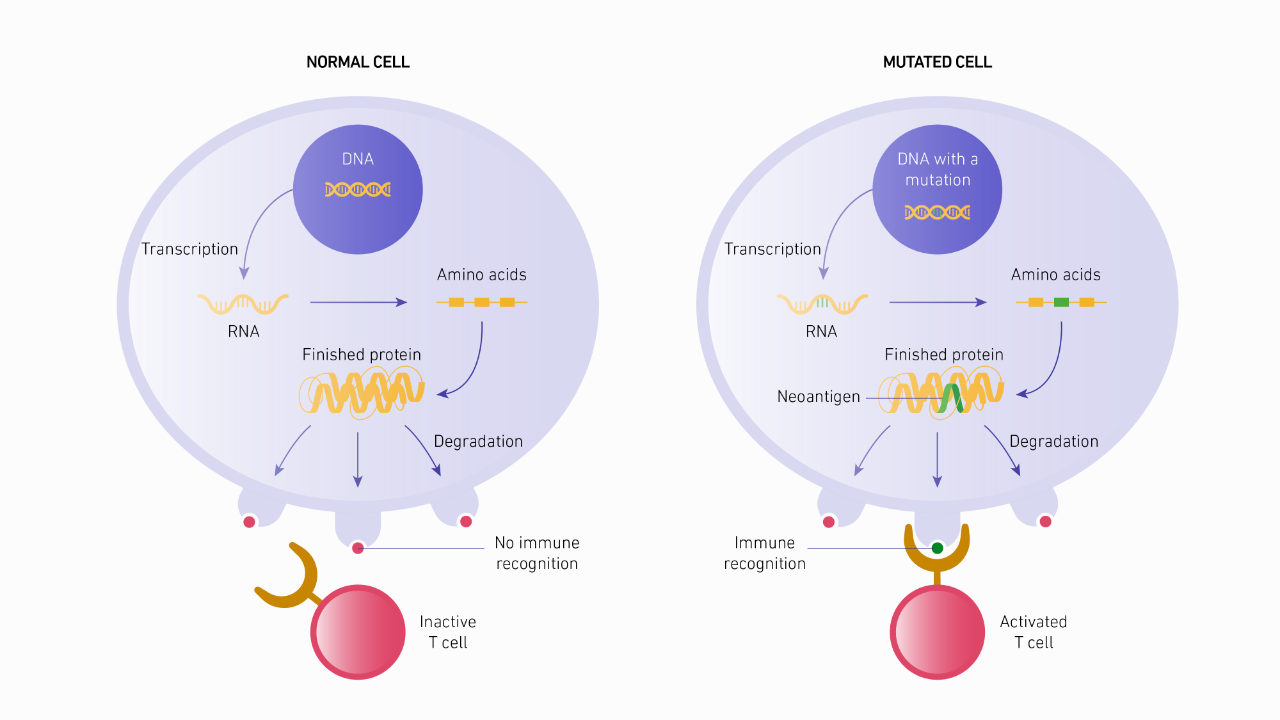
图源自Technology Networks
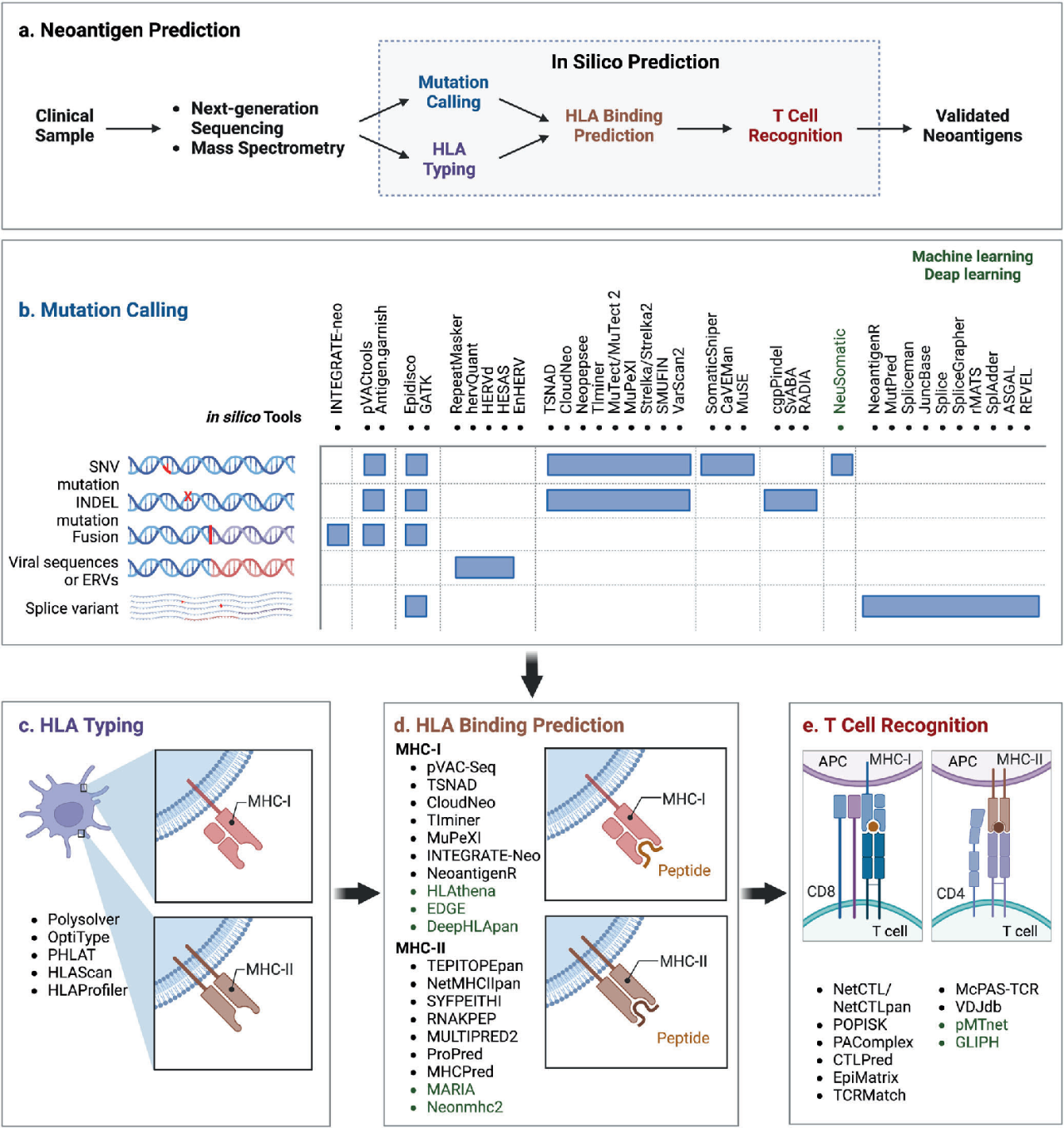
肿瘤新抗原预测流程【3】
个性化肿瘤mRNA疫苗如何发挥作用?
2025年8月8日,国家自然科学基金委员会发布赋能药物创新的RNA基础研究重大研究计划2025年度项目指南“关于发布赋能药物创新的RNA基础研究重大研究计划2025年度项目指南的通告”。指南开篇强调“面向RNA药物创制的国家重大需求”。2025年拟资助(培育项目30-40项 × 80万/项 + 重点支持项目3-5项 × 300万/项),申请书提交日期为2025年9月15日-2025年9月22日16时。
https://www.nsfc.gov.cn/publish/portal0/tab434/info95398.htm
为全面推进肿瘤mRNA疫苗的研究与产业化发展。表观生物与珲信生物达成战略合作协议。双方将聚焦肿瘤mRNA疫苗技术及其相关产品领域,展开深度战略合作。期望携手为推动中国生物医药产业的创新与发展贡献一份力量,造福肿瘤患者。
我们正式推出从肿瘤新抗原预测到mRNA-LNP制剂制备的一站式服务:
1. 经典方案
-
肿瘤组织:WES(15 G)+mRNA-seq(10G)
-
全血:WES(10 G)
分析内容:体细胞突变(Mutations)、单核苷酸突变(SNVs)、插入/缺失(InDels)、融合基因(Fusions)
2. 全基因组方案
-
肿瘤组织:WGS(90 G)+WES(15 G)+mRNA-seq(10 G)
-
全血:WGS(90 G)+WES(15 G)
分析内容:Mutations、SNVs、InDels、Fusions、结构变异(SVs)、拷贝数变异(CNVs)、异常剪接连接点(Junctions)
3. 联合翻译组方案
-
肿瘤组织:WES(15 G)+longRNA-seq(15 G)+Ribo-seq(100 M)
-
正常组织:longRNA-seq(15 G)+Ribo-seq(100 M)
-
全血:WES(10 G)
分析内容:Mutations、SNVs、InDels、Junctions、Fusions、肿瘤特异性翻译事件
NeoDesign序列优化与设计→基因合成→载体构建→质粒生产
模版制备→体外转录(IVT)→纯化与质控→批次扩增
LNP配方设计→mRNA-LNP封装→纯化与浓缩→GMP生产
研究方案与案例
经典方案:WES+mRNA-seq
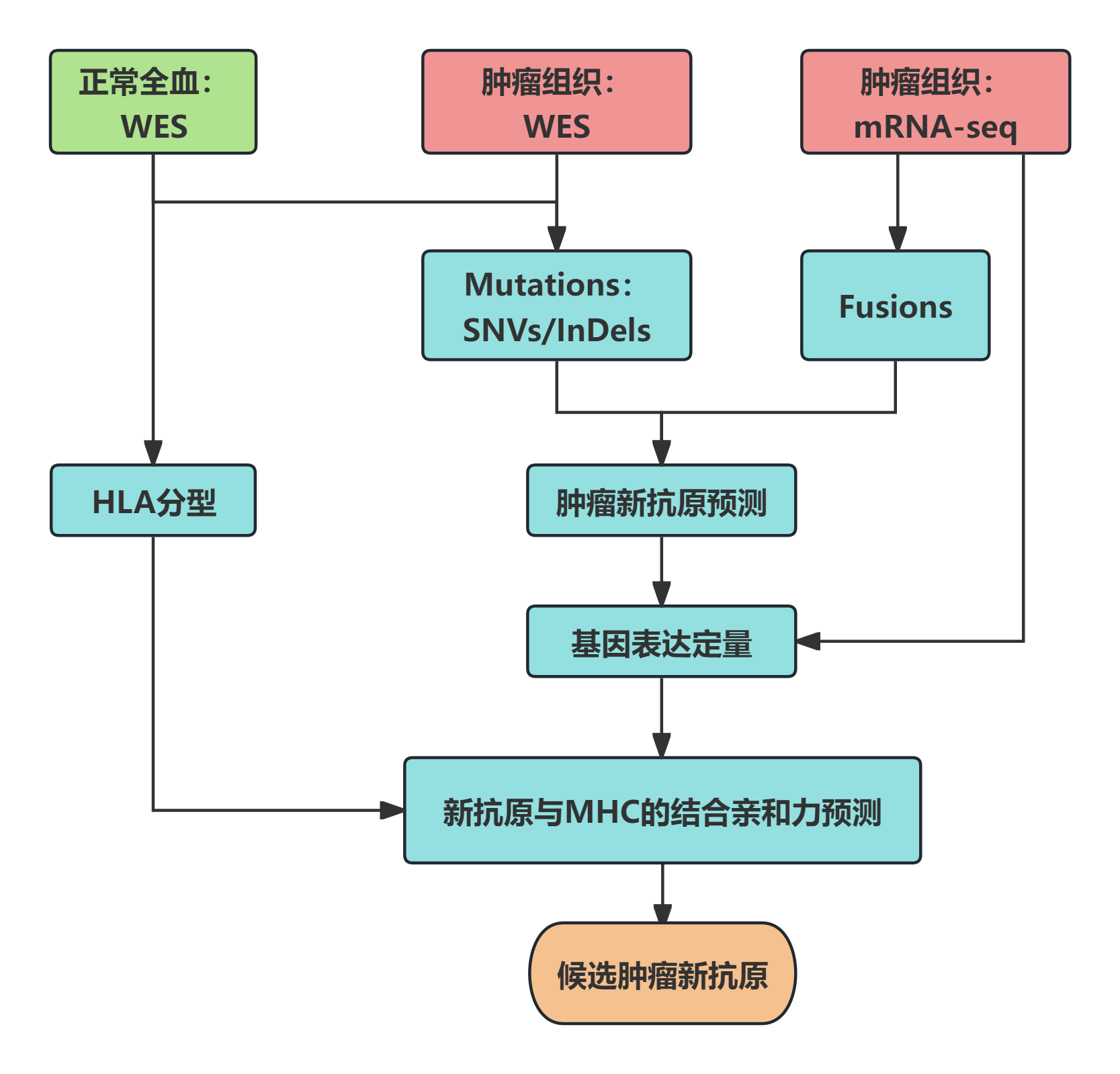
WES全外显子测序专注编辑蛋白质的区域,即外显子组。这部分虽然只占整个基因组的1~2%,但包含了大约85%的致病突变[4]。WES检测突变,mRNA-seq检测突变基因的转录表达水平。
优势:成本较低,分析流程成熟。
局限:WES无法发现非编码区突变或较大结构变异,错过潜在的新抗原来源;mRNA-seq不能直接证明突变蛋白被翻译或呈递。
📑研究案例:
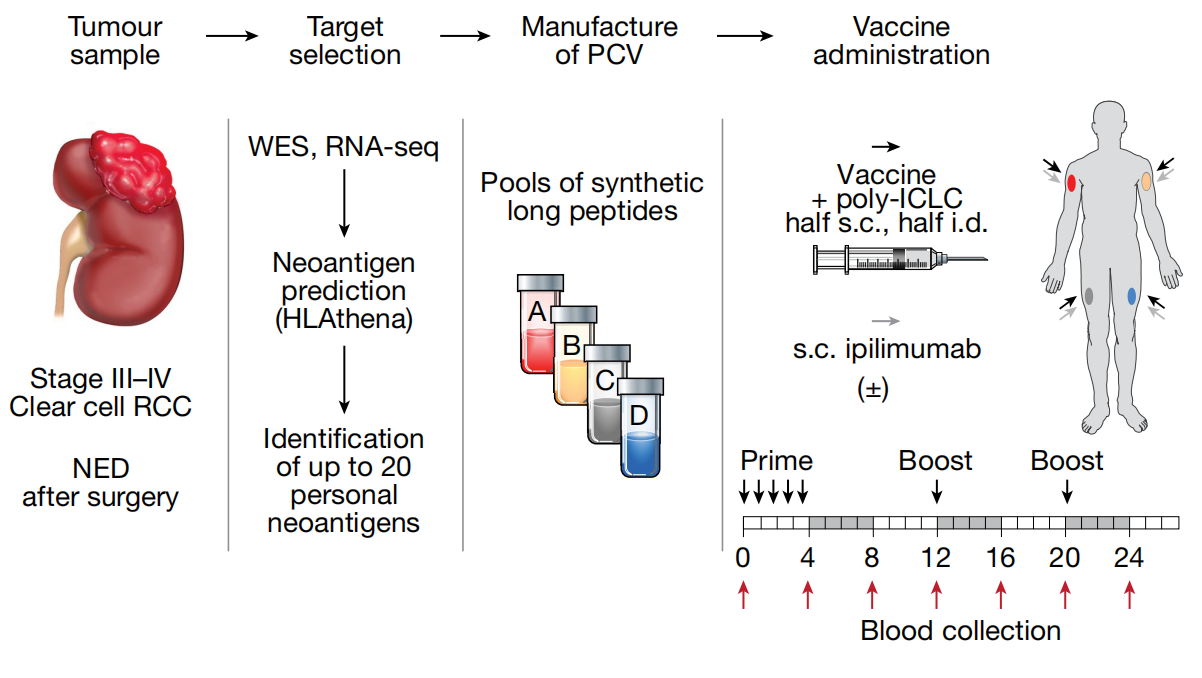
1. 《Nature》A neoantigen vaccine generates antitumour immunity in renal cell carcinoma[5]
这项I期临床试验研究了个性化新抗原疫苗在9名高风险肾细胞癌患者中的应用,通过WES和RNA测序识别体细胞突变,优先选择驱动基因突变、高表达、克隆性突变等高质量新抗原,设计成15-33个氨基酸的合成长肽并分为4个肽池制备疫苗。结果显示,中位随访40.2个月后无一例患者复发,所有患者均产生了针对疫苗抗原的T细胞免疫反应,包括对VHL、PBRM1、BAP1等关键驱动基因突变的反应,77.8%的患者检测到抗自体肿瘤反应性,证明了个性化新抗原疫苗在低突变负荷肿瘤中的可行性和免疫原性。
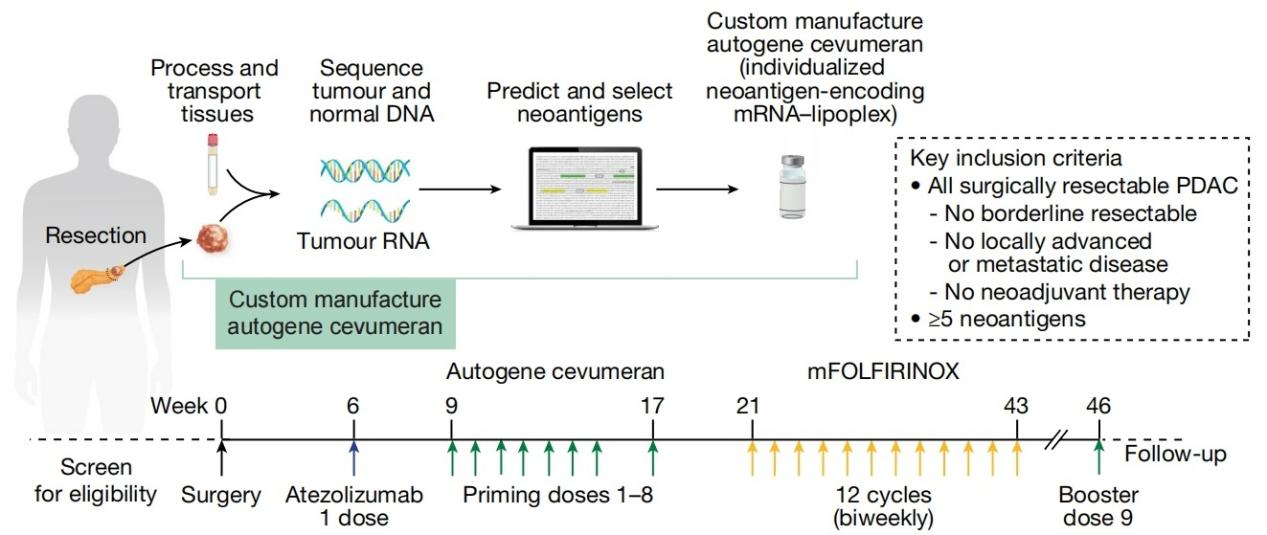
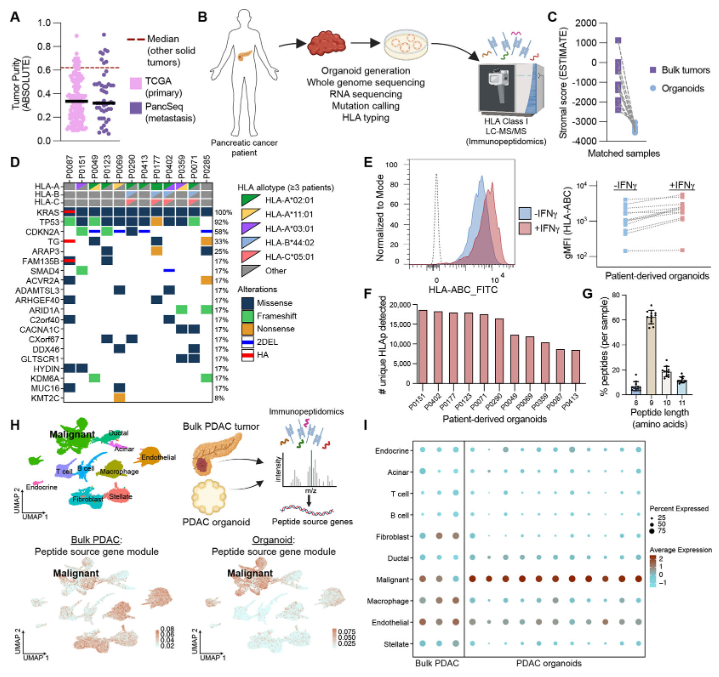
2. 《Nature》Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer[6]
这项研究使用WES识别体细胞突变、RNA-seq确认突变基因表达、HLA分型确定限制性元件,结合生物信息学算法预测和排序新抗原免疫原性,成功开发出个体化mRNA新抗原疫苗治疗胰腺癌。研究还创新性地运用TCR Vβ测序开发CloneTrack方法追踪疫苗扩增的T细胞克隆,并通过单细胞RNA/TCR测序深入分析T细胞功能,证明了该疫苗能有效激活新抗原特异性T细胞应答并显著延长患者无复发生存期。
全基因组方案:WGS+WES+mRNA-seq
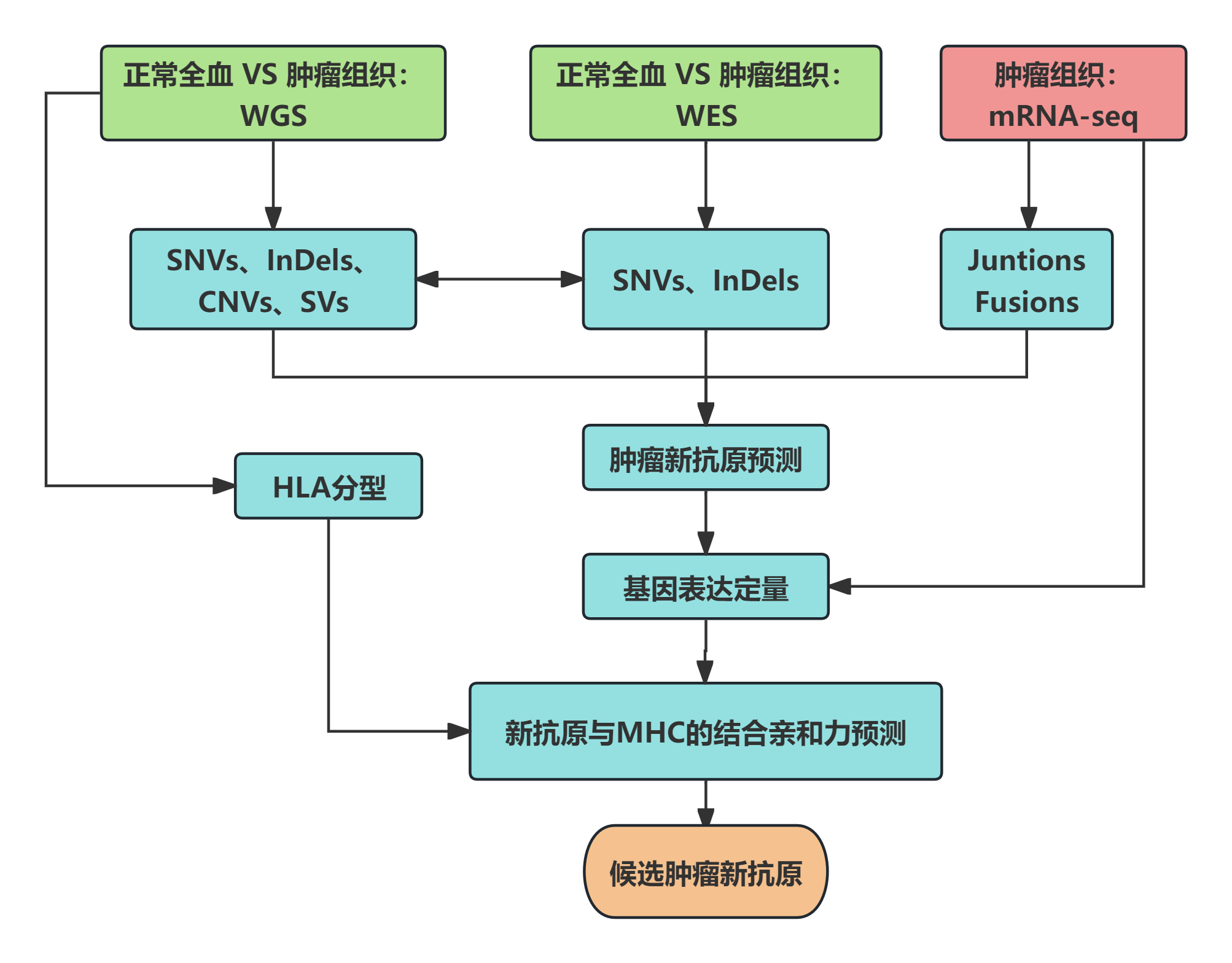
WGS覆盖全基因组,可以检测非编码区、SVs和CNVs,能发现WES遗漏的内部SV、基因融合断点和可变剪接位点[7,8]。
优势:检测全基因组范围所有突变,包括非编码区的新抗原。
局限:成本稍高、数据量大、分析时间延长
📑研究案例:
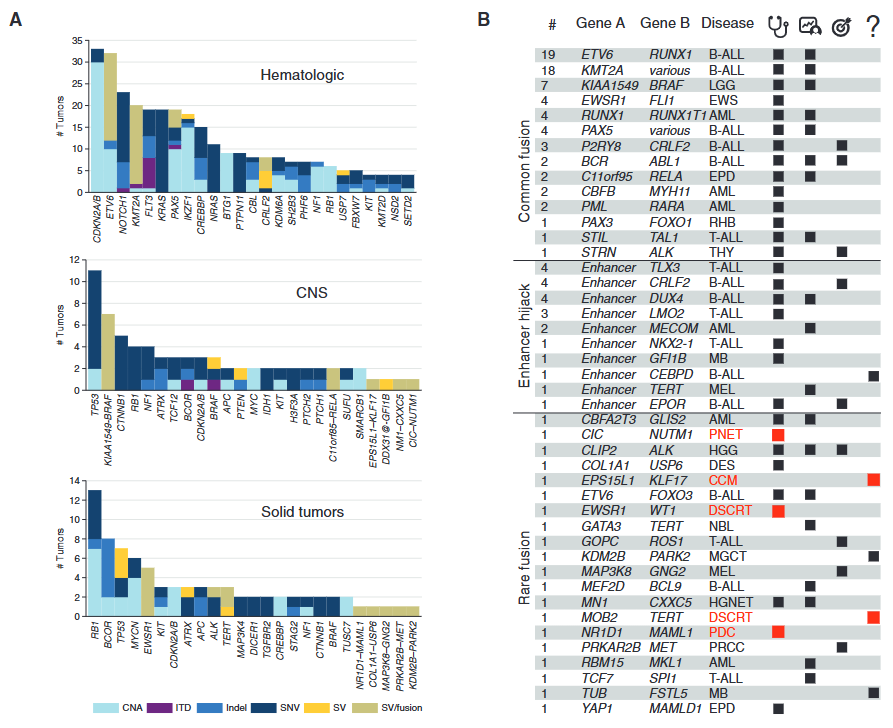
1. 《Cancer Discovery》Genomes for Kids: The Scope of Pathogenic Mutations in Pediatric Cancer Revealed by Comprehensive DNA and RNA Sequencing[9]
这项研究通过三组学联合分析(WGS、WES、RNA-seq)对309例儿童癌症患者进行综合突变分析。研究在体细胞突变层面检出平均每例3个致病性变异,包括基因融合(36%)、增强子劫持(8%)和微缺失(15%)等复杂结构变异;在胚系突变分析中发现18%患者携带癌症易感变异,其中55%与肿瘤发生直接相关。三组学联合的核心优势在于WGS检测结构变异和非编码区突变,WES精确识别编码区点突变,RNA-seq验证功能影响和异常表达,相互补充实现了比单一测序平台更全面的突变谱解析,最终86%患者获得临床可操作的基因组信息。
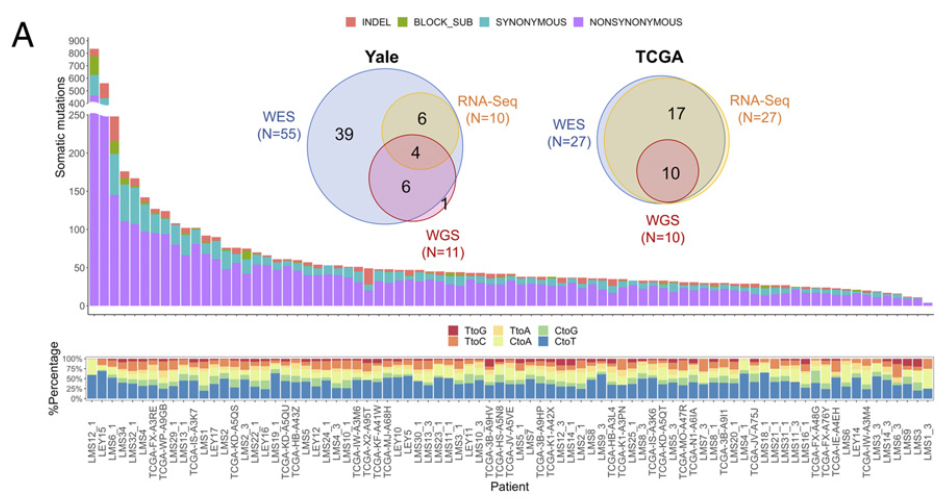
2. 《PNAS》Integrated mutational landscape analysis of uterine leiomyosarcomas[10]
这篇研究采用WGS、WES和RNA-Seq三种测序技术的整合分析策略,对83例子宫平滑肌肉瘤进行了全面的基因组学分析。研究通过联合突变分析识别了体细胞SNV、InDel、CNV、Fusion和SV等多层次基因组改变,发现TP53(43.9%)、ATRX(30.4%)、PTEN(4.9%)和新识别的MEN1(6.1%)为显著突变的驱动基因。突变特征分析揭示25%的肿瘤具有同源重组修复缺陷(HRD)特征,2%具有微卫星不稳定(MSI)特征,76%的样本存在染色体复杂重排。基于这些分子特征,研究通过PDX模型验证了PARP抑制剂、BET抑制剂和PI3K抑制剂的治疗潜力,为子宫平滑肌肉瘤的精准治疗提供了重要的基因组学依据。
联合翻译组方案:WES+longRNA-seq+Ribo-seq
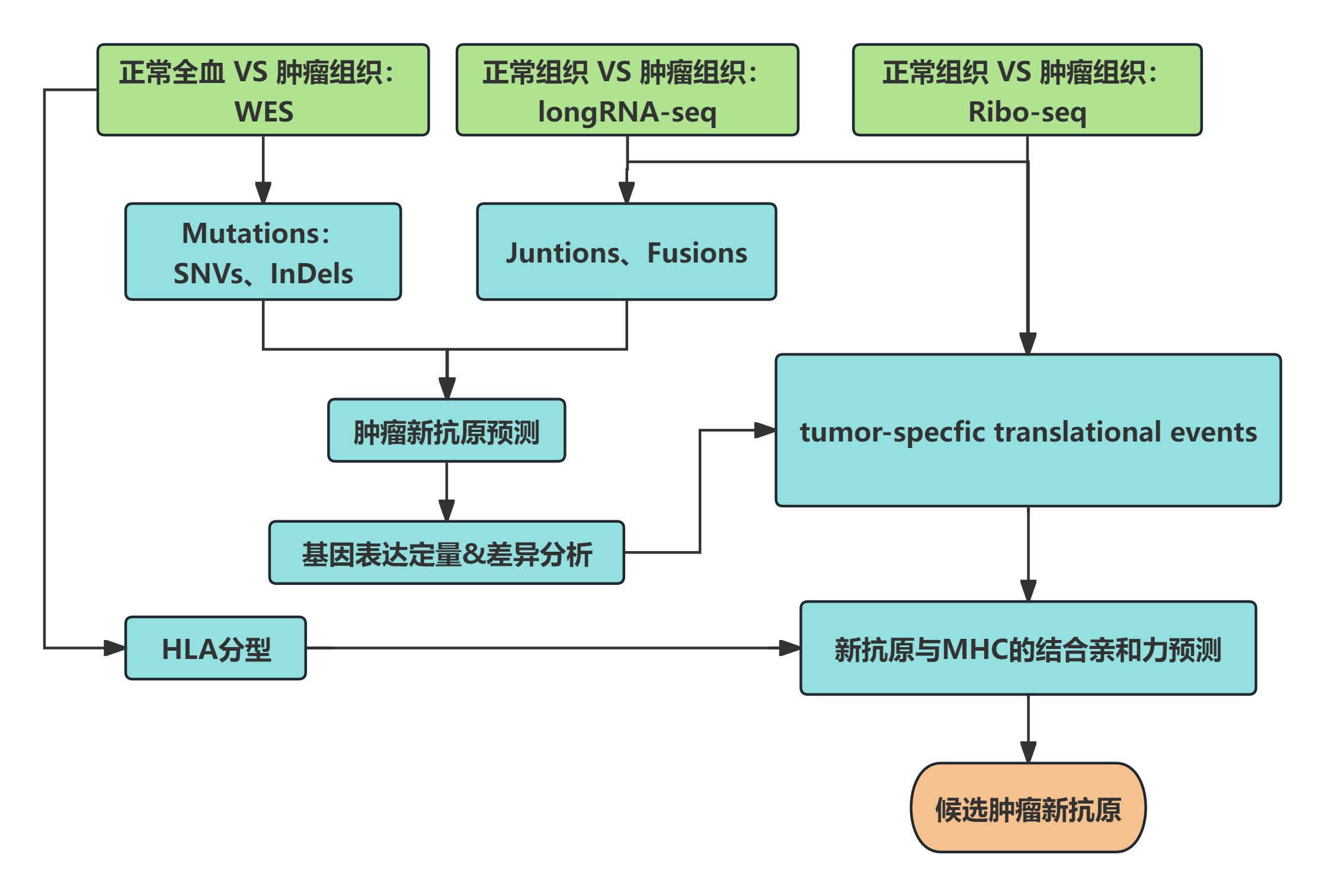
2025年5月,麻省理工在《Science》发表了关于胰腺癌隐秘抗原的文章,该研究发现了胰腺癌中由HLA-I分子呈递的非典型抗原肽,这些抗原主要来源于lncRNA、UTR及内含阅读框,具有高度的癌症特异性[11]。longRNA-seq可用时检测mRNA和lncRNA;Ribo-seq可提供突变肽段真实翻译的证据;过滤掉未翻译的突变肽段;鉴定难以识别的非经典开放阅读框等;发现遗漏的潜在新抗原等[12]。
优势:最大限度挖掘新抗原来源,可发现非经典ORF翻译出的肽段;增强候选新抗原的可信度,降低假阳性率[13]。
局限:样本要求严格,成本稍高,数据分析复杂。
📑思路参考:
1. 《Science》:Pancreatic cancer-restricted cryptic antigens are targets for T cell recognition[11]
该研究首次系统性地证明了胰腺癌中存在大量癌症特异性的隐性抗原,这些来源于非编码基因组区域的肽类分子具有良好的免疫原性,可作为新的免疫治疗靶点。这为突变负荷较低的胰腺癌等实体瘤提供了全新的免疫治疗策略,有望扩大癌症免疫治疗的适用范围,特别是对传统免疫检查点抑制剂治疗无效的患者群体。
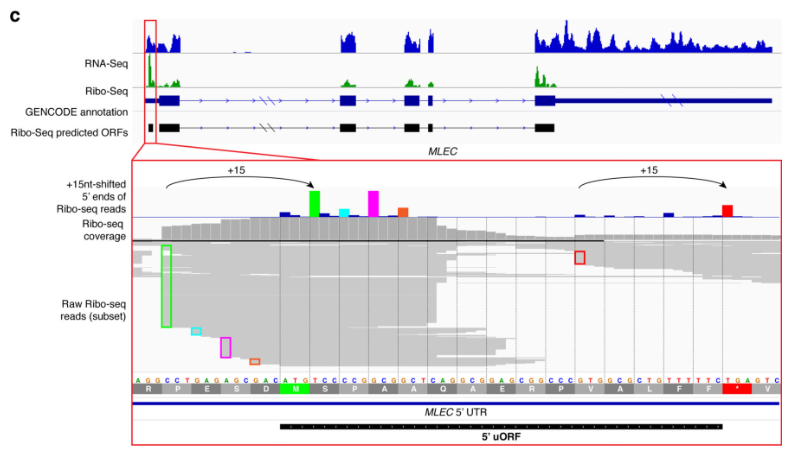
2. 《Nat Biotechnol》:Unannotated proteins expand the MHC-I-restricted immunopeptidome in cancer[12]
这项研究通过结合核糖体分析和质谱技术,发现了数千个来自未注释开放阅读框(nuORFs)的MHC-I呈递肽段,证明nuORFs可作为癌症特异性抗原的重要来源,通过体细胞突变和癌症富集翻译两种机制扩展了潜在的新抗原库,为癌症免疫治疗提供了新的靶点和策略。
3. 《Nat Commun》:Global proteogenomic analysis of human MHC class I-associated peptides derived from non-canonical reading frames[14]
该研究首次系统性地证明了约10%的人类MHC-I类呈递肽段来源于基因组的非编码区域或非规范翻译,这些隐性肽段具有独特的生物学特征和免疫学性质,显著增加了免疫肽组的复杂性,扩展了CD8+ T细胞免疫监视的范围,为肿瘤免疫治疗中寻找新型肿瘤抗原提供了重要的理论基础和技术路径。
多价肿瘤新抗原mRNA疫苗(如结合20-30个抗原肽)可增强免疫原性,但序列设计面临挑战:多肽随机组合和同义密码子会产生海量序列选项,导致linker过多、意外新抗原生成、复杂蛋白结构和mRNA不稳定等问题。这些可能降低疫苗的安全性和效能(如免疫逃逸或降解加速)。
NeoDesign[15]工具可从多肽组合生成的序列池中选择最优蛋白序列,并为后续mRNA序列设计提供指导。
候选的肿瘤新抗原输入NeoDesign(通常10-30个),输出最优蛋白序列和λ建议。NeoDesign的流程分为四个模块:
-
Library Construction(库构建)
-
Optimal Path Filtering(最优路径过滤)
-
Linker Addition(连接子添加)
-
λ-Evaluation(λ评估)
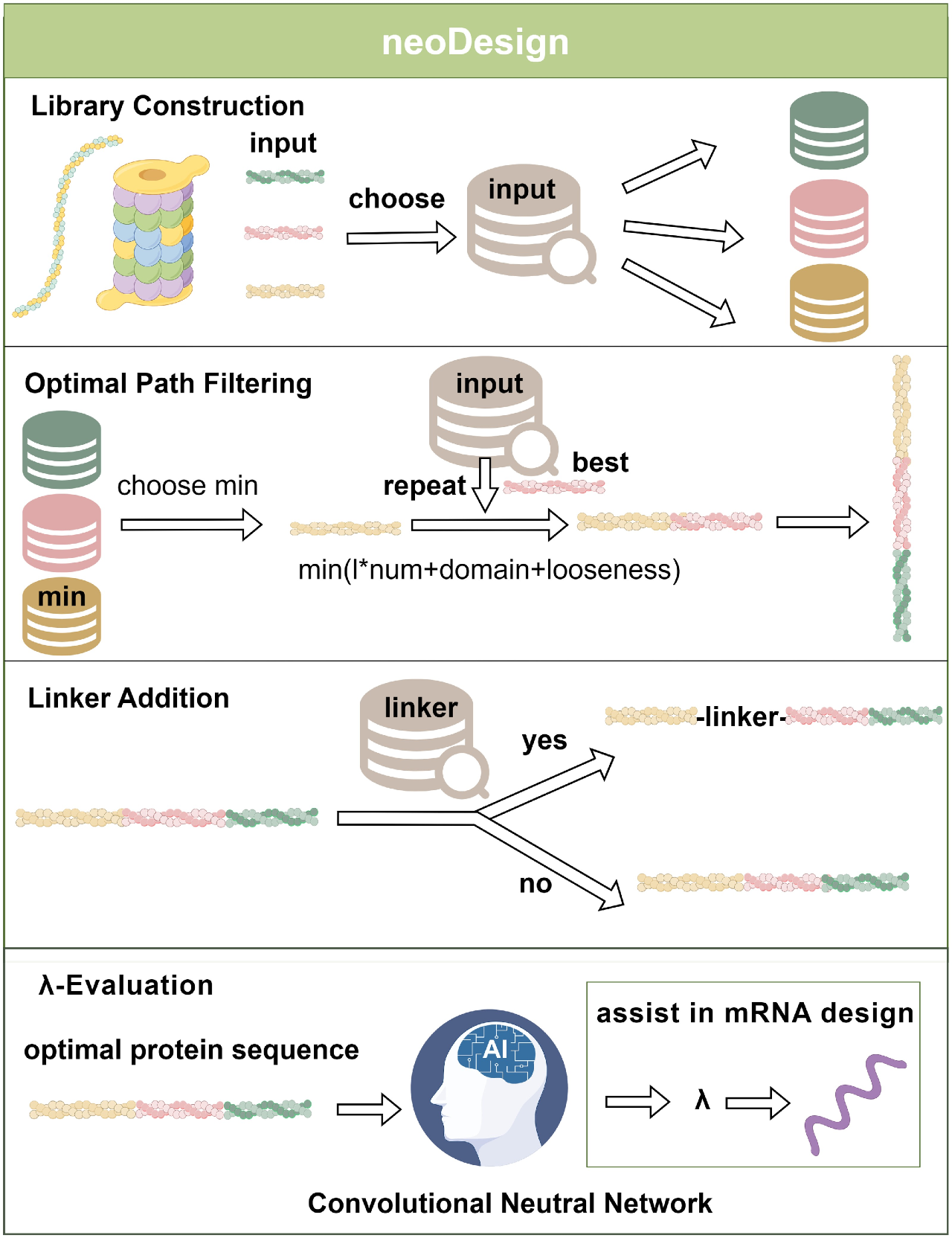
NeoDesign的架构[15]
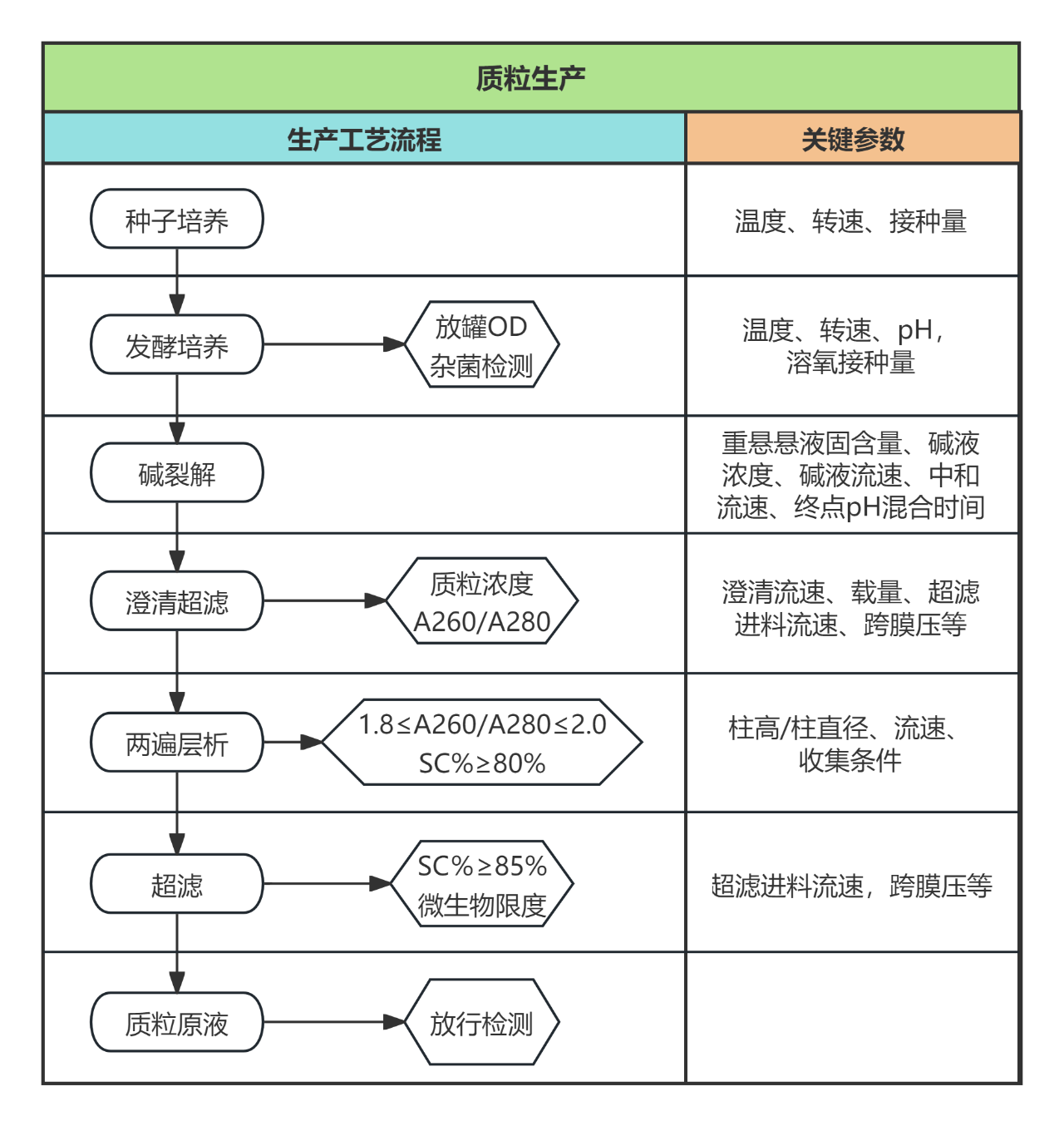
质粒生产
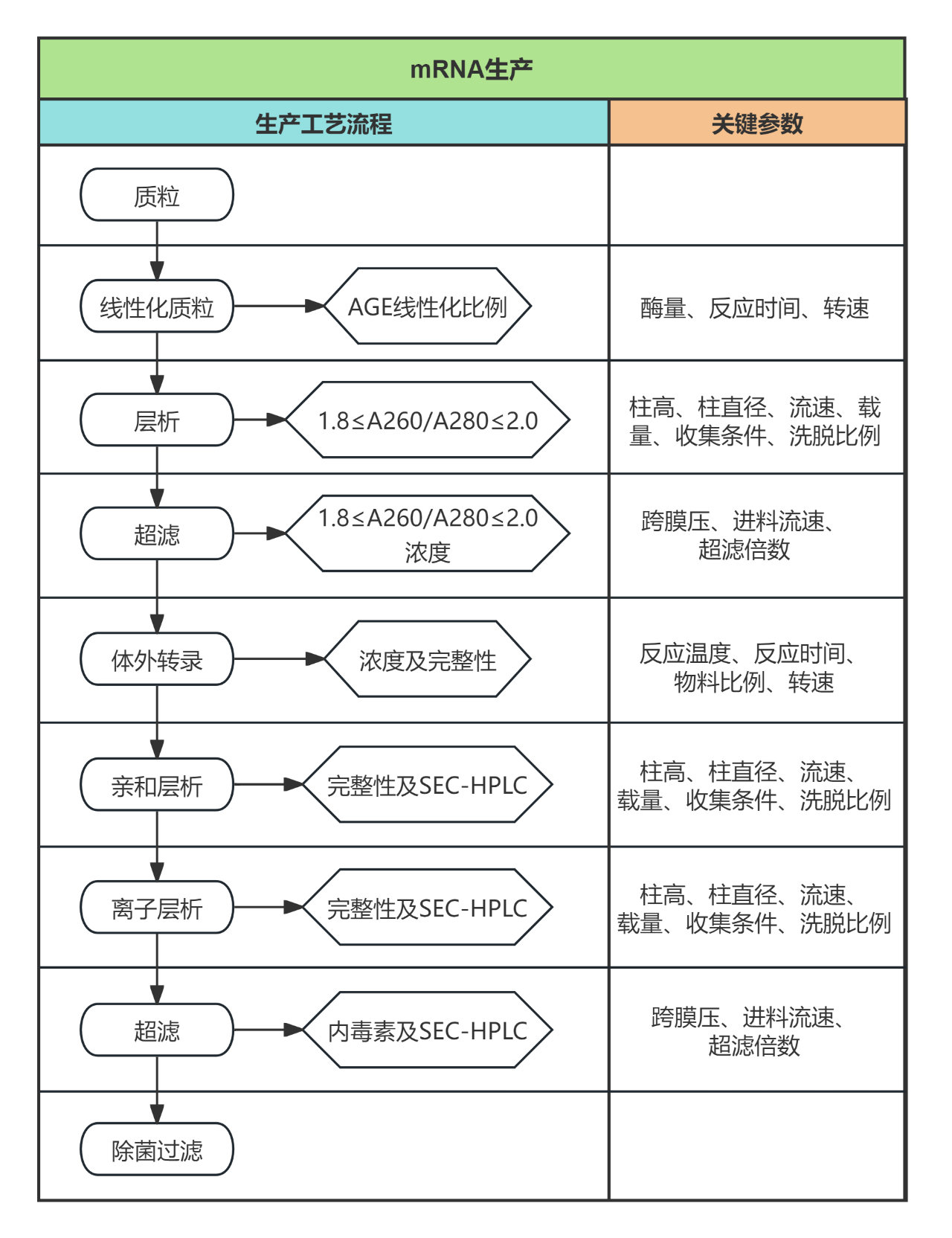
mRNA生产
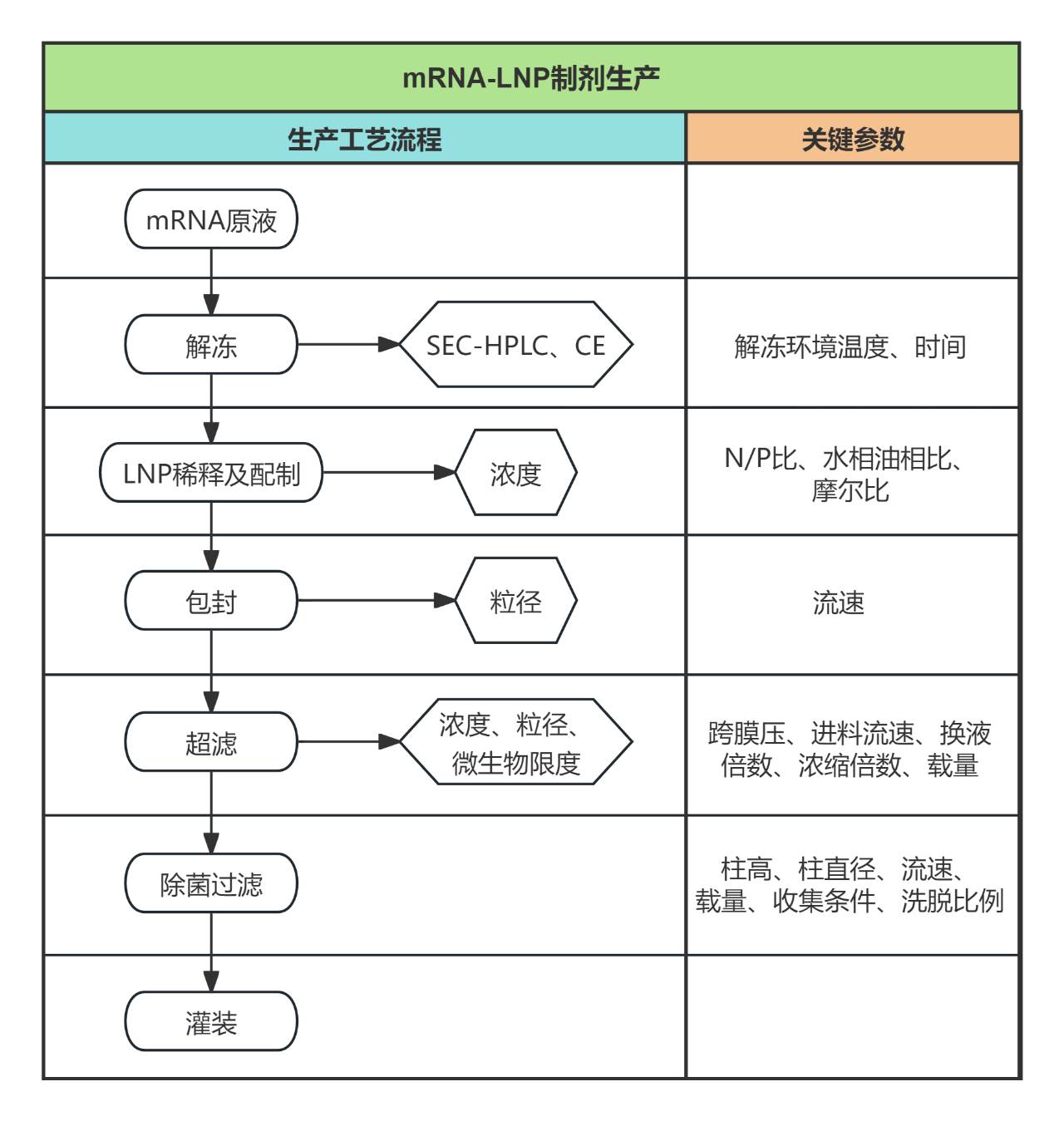
mRNA-LNP生产