蛋白相分离

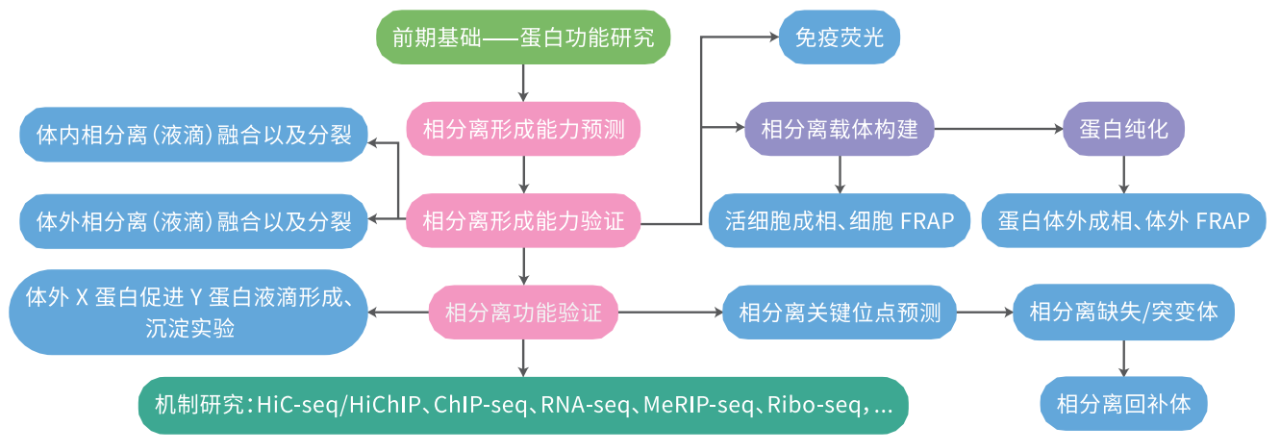
一、蛋白相分离形成能力预测
蛋白相分离形成能力预测
通过生物信息学的前沿算法,可以对蛋白相分离形成能力进行一个初步的预测。
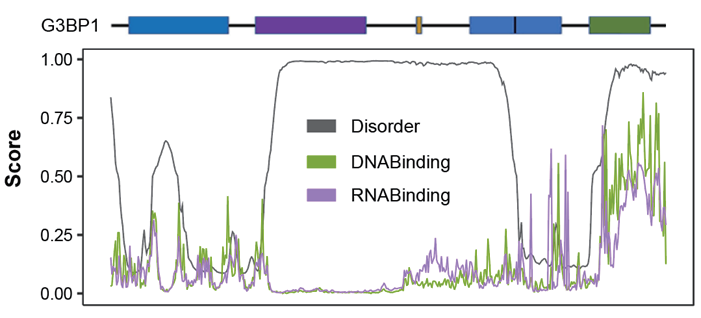
内容:利用机器学习建立的PSPHunter算法,基于蛋白氨基酸序列,整体预测蛋白相分离形成能力(赋分0.8以上为高成相能力蛋白)
二、蛋白相分离形成能力验证
细胞中最为常见的相分离是液态相分离结构。目前相分离研究领域认为[4],鉴定相分离,需要以下的实验证明:
1. FRAP
2. 结构大小是否达到或接近微米级别
3. 活细胞成像
4. 体外重构
有鉴于此,表观生物推出了以下的蛋白相分离形成能力验证实验服务:
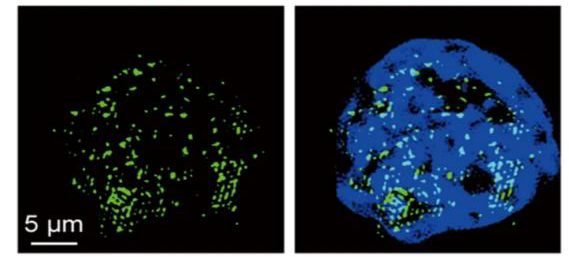
免疫荧光染色检测蛋白细胞分布
内容:通过免疫荧光染色,检测目的蛋白的活细胞分布以及聚集情况。可同时检测两个蛋白的活细胞分布以及共定位情况(需要客户提供细胞以及目的蛋白抗体)
相分离荧光载体构建
内容:
原核表达纯化及蛋白体外成相实验
2012年,美国西南医学中心的研究团队发现在试管中分子通过微弱的作用力形成液滴,首次证实了相分离能够通过简单的生化实验在体外重复[5]。因此,相分离可以在体外通过纯化的蛋白以及核酸等在特定的条件下发生,体外重构的相分离实验对于该领域具有重要的作用。
内容:原核表达融合His-Tag以及荧光Tag的目的蛋白,经过镍柱亲和纯化,获得高纯度的目的蛋白。摸索适合的体外成相条件,观察目的蛋白的体外成相情况

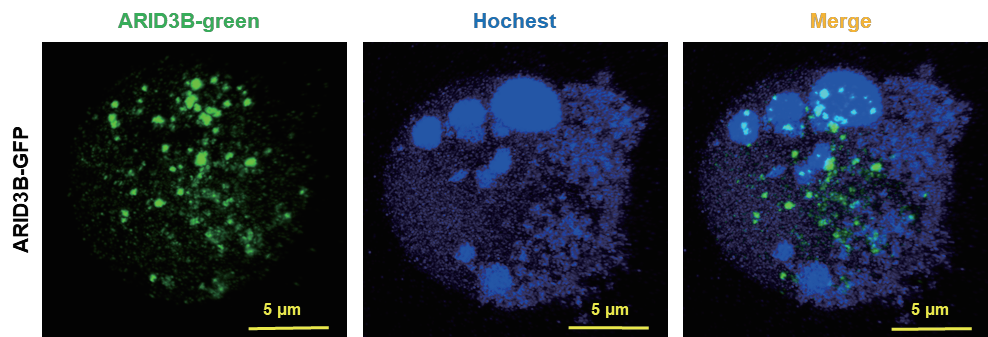
蛋白融合荧光细胞系构建以及活细胞成相实验
内容:将目的蛋白融合荧光蛋白(EGFP/RFP)真核表达载体转染至目标细胞中,经过药物筛选构建稳定表达细胞系。利用构建成功的细胞系进行激光共聚焦活细胞成像,观察目的蛋白在细胞内成相情况。
体外FRAP
荧光漂白恢复实验(fluorescence recovery after photobleaching,FRAP)常用于测量液滴的流动性,看所研究的蛋白是否在短时间内恢复荧光,这可以表明此种结构是否与周围环境在进行频繁的物质交换,辅助验证相分离。
内容:蛋白在体外体系形成相分离后,使用激光共聚焦显微镜观察相分离液滴经过光漂白之后,液滴淬灭区域荧光恢复情况,由此验证蛋白体外相分离液滴的流动性
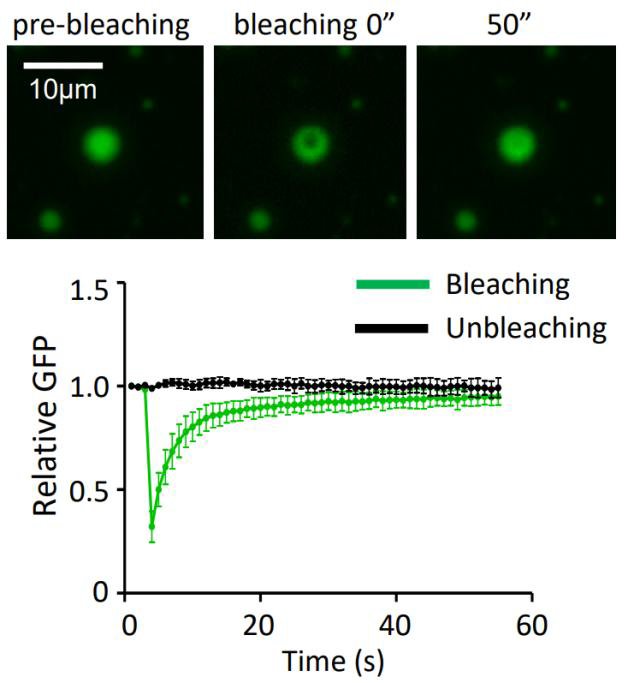
细胞内FRAP
一个相分离结构验证标准:形成球状结构,能够融合,通过FRAP技术可证明其能够发生荧光漂白恢复。
内容:对于活细胞内形成的相分离液滴,使用激光共聚焦显微镜观察相分离液滴经过光漂白之后,液滴淬灭区域荧光恢复情况,由此验证细胞内相分离液滴的流动性。
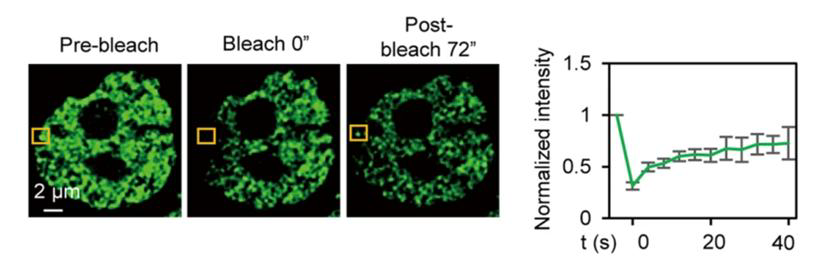
体外相分离融合及分裂
内容:蛋白在体外体系形成相分离后,使用激光共聚焦显微镜长时间拍摄模块,观察相分离液滴的融合及解聚现象,由此验证体外相分离液滴的流动性
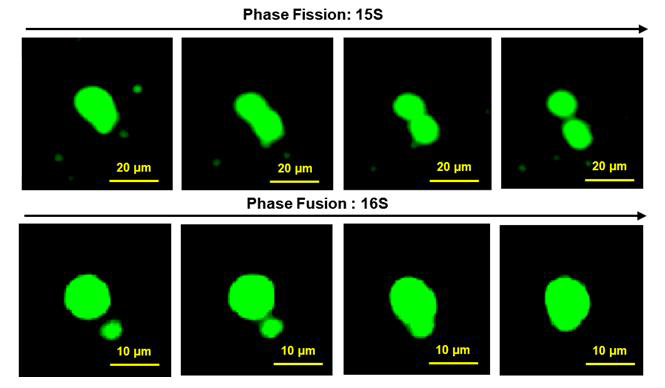
细胞内相分离融合及分裂
活细胞成像实验,目的是观察液滴融合或分离现象。
内容:对于活细胞内形成的相分离液滴,使用激光共聚焦显微镜长时间拍摄模块,观察相分离液滴的融合及解聚现象,由此验证细胞内相分离液滴的流动性
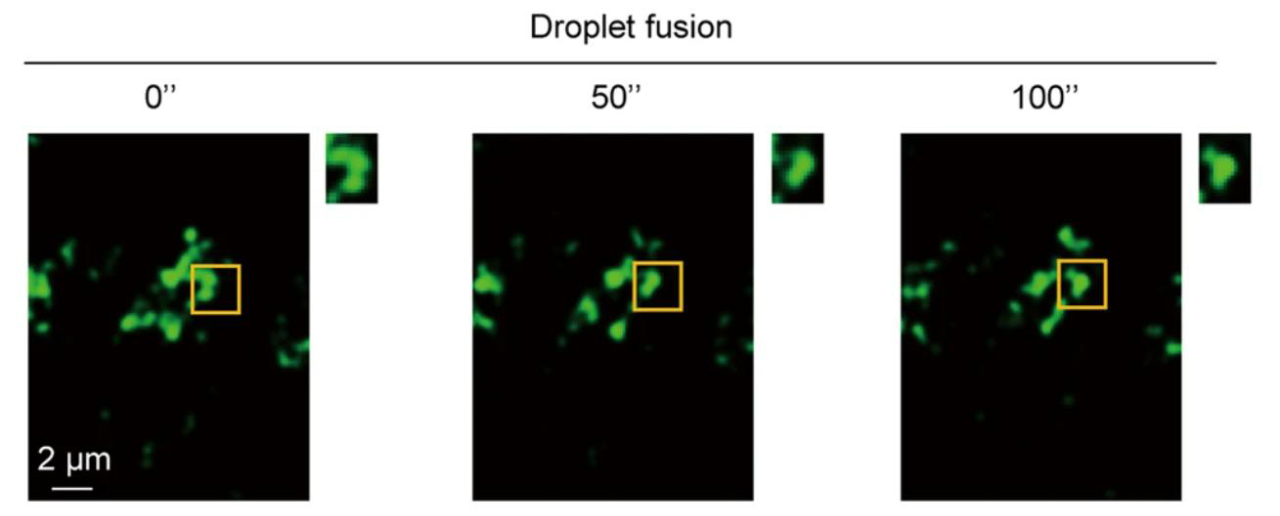
三、蛋白相分离功能验证
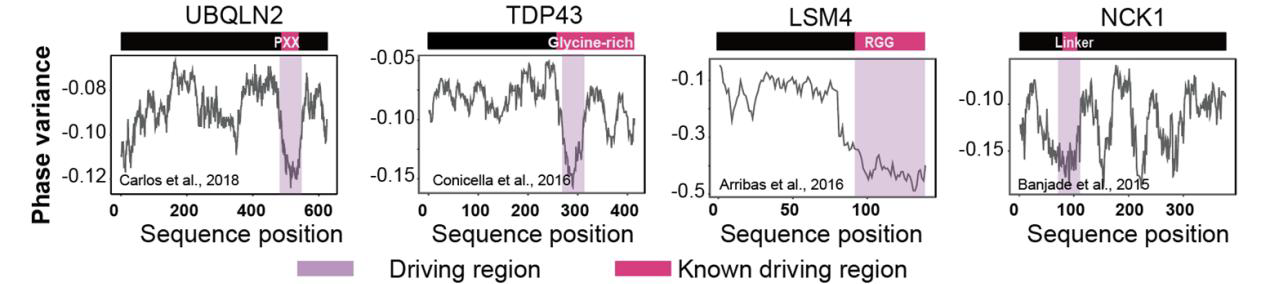
蛋白关键相分离位点预测
内容:利用机器学习建立的PSPHunter算法,基于蛋白氨基酸序列,识别蛋白的关键相分离驱动氨基酸区段
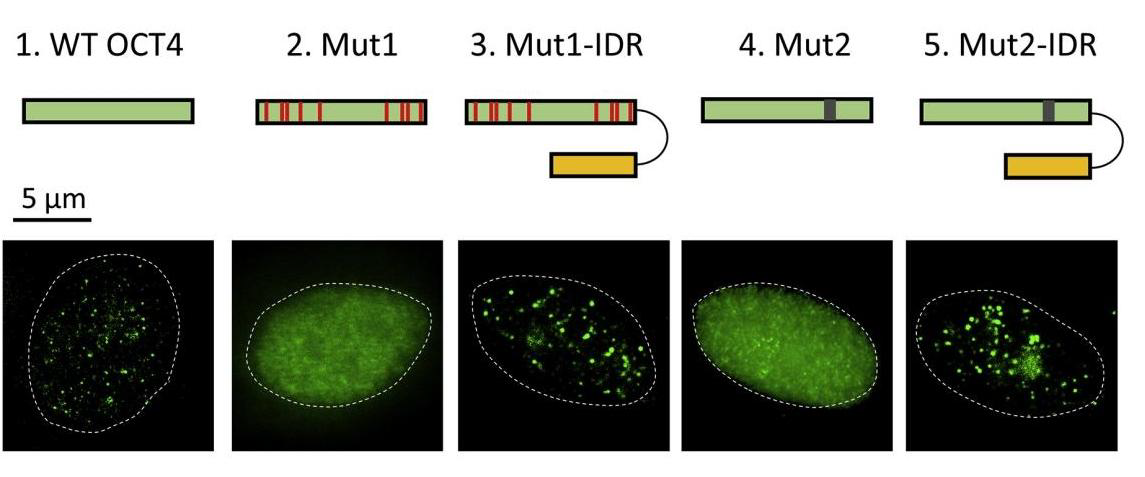
蛋白成相突变体以及突变回补体构建及成像验证
为了验证相分离对于蛋白功能的直接影响,我们通常需要在破坏蛋白成相能力以及回补其成相能力之后,进行功能性的验证。
内容:在获得蛋白关键成相位点信息之后,在避开蛋白重要的功能性结构域的前提下,对于蛋白关键成相位点设计突变,破坏其相分离形成能力,并且通过融合表达已知具有相分离形成能力的蛋白无序区短肽(例如FUS IDR、hnRNPac1 IDR、polyG等)进行成相能力回补。而后,通过构建相关真核及原核表达载体,并且在细胞内以及体外对于成相突变体的成相能力进行验证。
四、蛋白与蛋白相互作用促进相分离功能验证
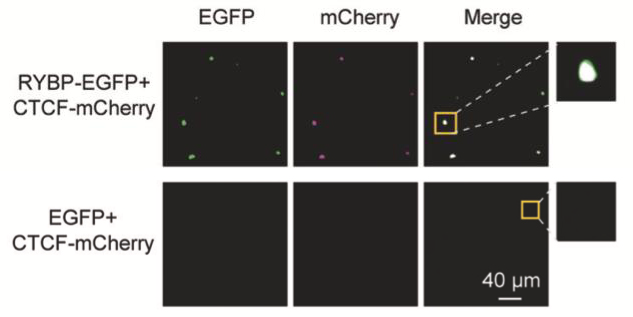
体外X蛋白促进Y蛋白相分离
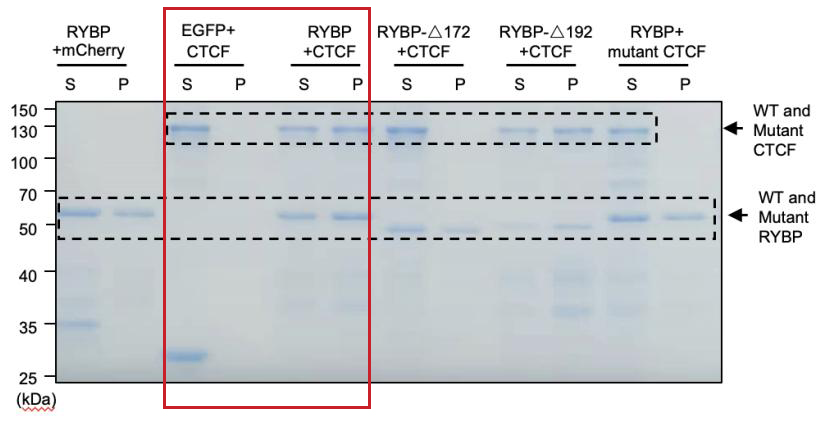
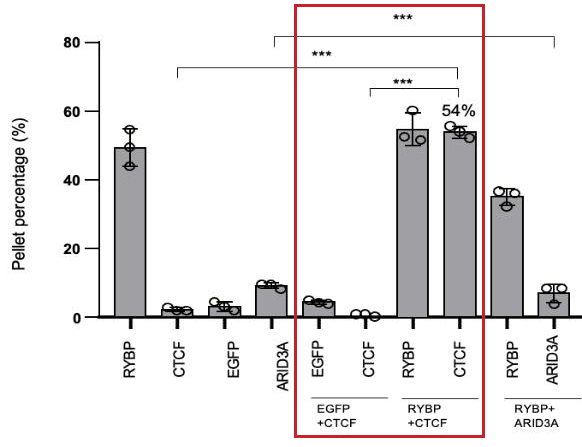
范例:RYBP体外促进CTCF相分离
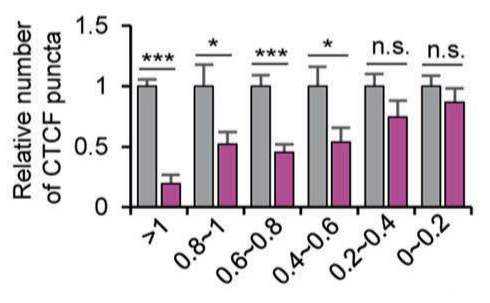
体外X蛋白促进Y蛋白相分离沉淀实验
范例:RYBP体外促进CTCF相分离沉淀实验
五、TurboID鉴定相分离互作蛋白
传统方法(如免疫沉淀)在鉴定动态、瞬时、弱相互作用蛋白质方面存在局限性,包括无法呈现真实状态、会破坏瞬时相互作用和无膜细胞器等。
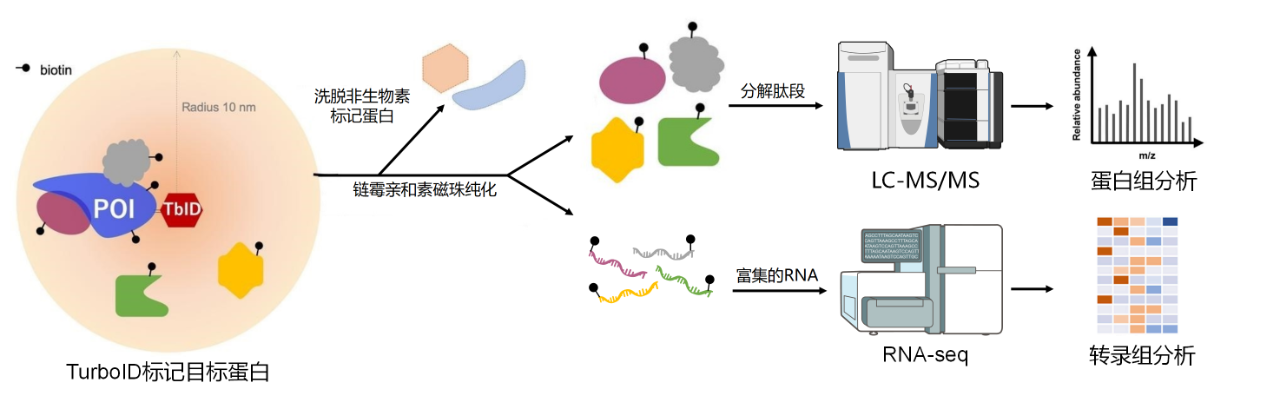
TurboID 邻近标记技术可在室温下直接在活细胞中加入无毒的生物素(biotin),对目标蛋白及其邻近蛋白进行快速标记(≥ 10 min),对细胞干扰小,标记尺度更短(~10 nm)等特点,在同类邻近标记技术(如 APEX、BioID 等)中表现最优。
通过 TurboID 标记后的蛋白复合物,可分解肽段进行 LC-MS/MS,也可富集 RNA 进行转录组测序(例图15)。蛋白组分析和转录组分析结果示例如例图16和例图17所示。
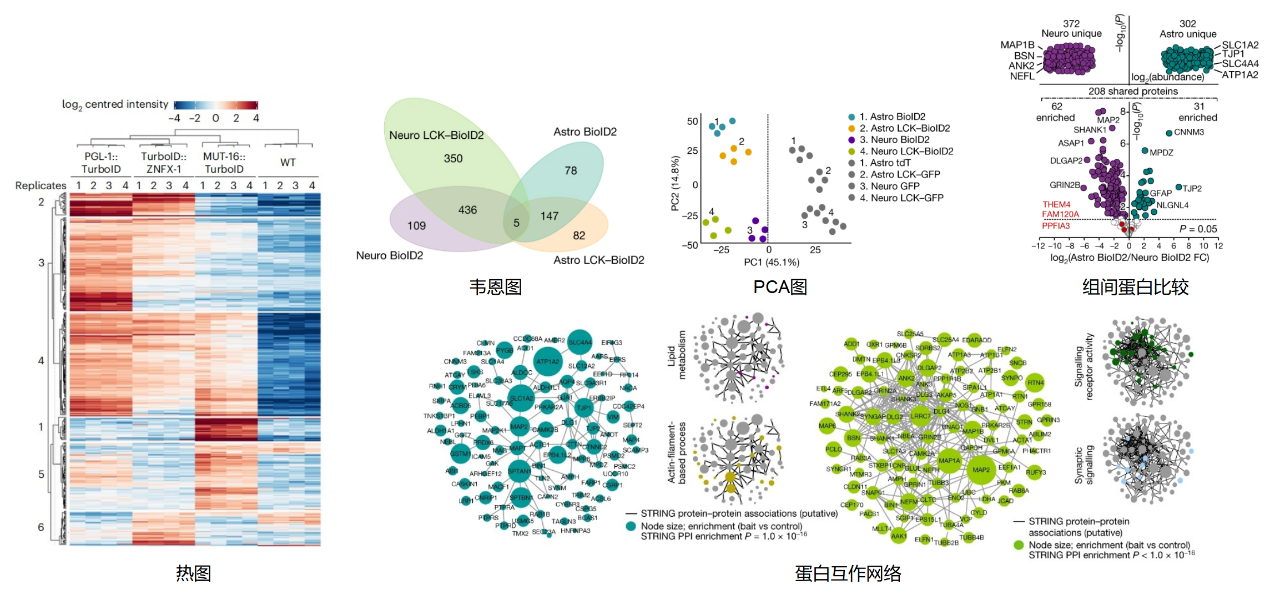
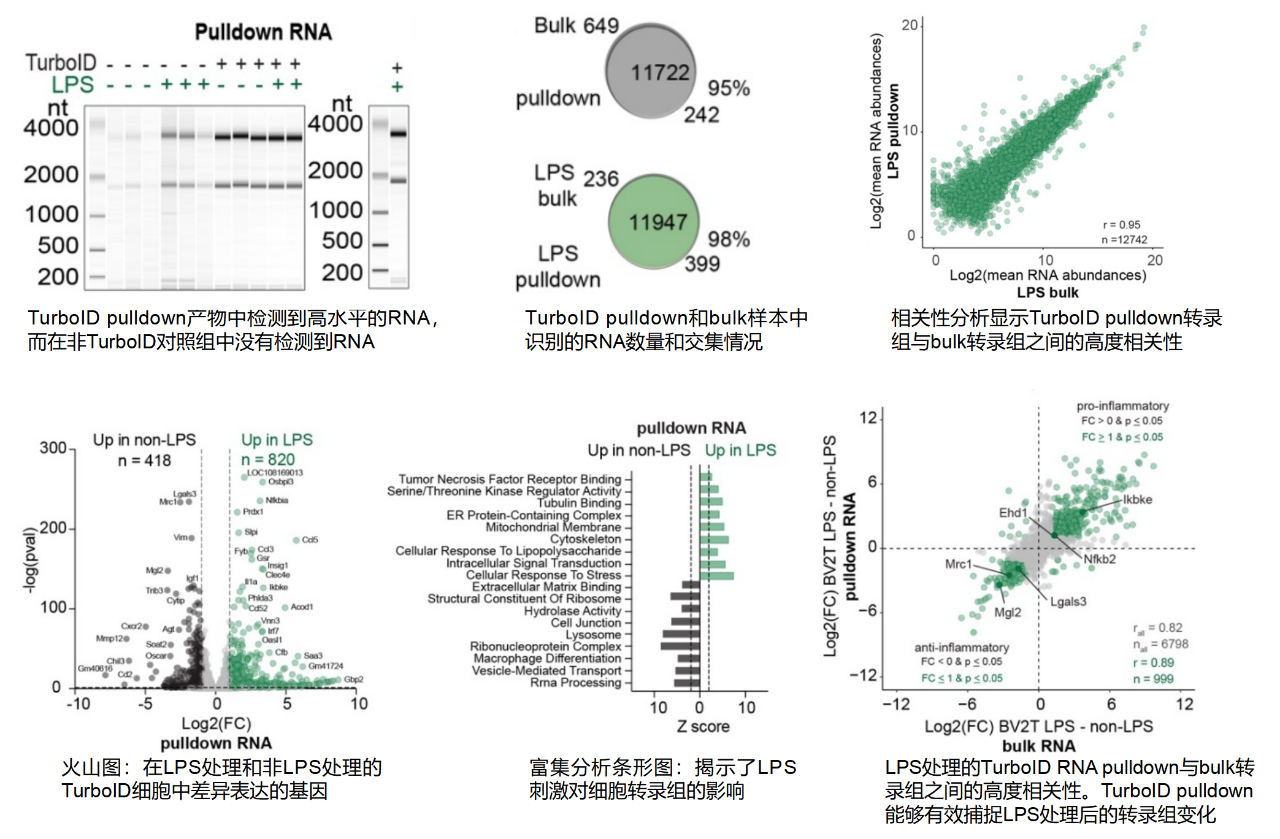
TurboID 技术服务主要内容包括:
-
生物素标记效率验证(Western Blot)
-
液滴共定位验证(免疫荧光成像)
-
液滴互作蛋白图谱构建(定量蛋白质组学)
-
液滴互作转录组测序
服务项目列表
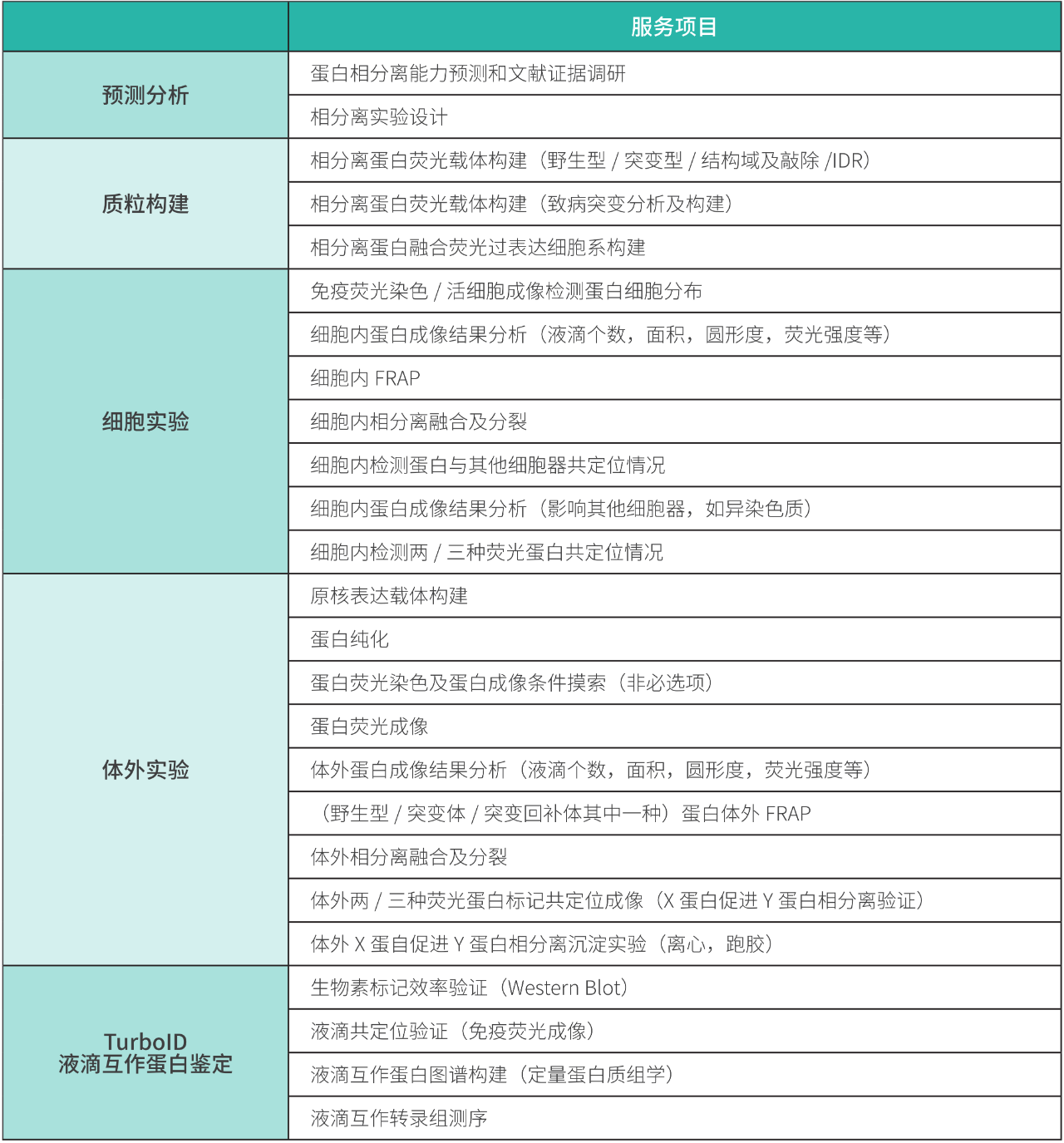

广州表观生物科技有限公司
TEL:400-775-0875
参考文献:
1. C. P. Brangwynne et al., Germline P granules are liquid droplets that localize by controlled dissolution/condensation. Science 324, 1729-1732 (2009).
2. S. F. Banani, H. O. Lee, A. A. Hyman, M. K. Rosen, Biomolecular condensates: organizers of cellular biochemistry. Nat Rev Mol Cell Biol 18, 285-298 (20 17).
3. M. Kato et al., Cell-free formation of RNA granules: low complexity sequence domains form dynamic fibers within hydrogels. Cell 149, 753-767 (2012).
4. Berry, J et al., Physical principles of intracellular organization via active and passive phase transitions. Reports on Progress in Physics, 81(4), 046601(2018).
5. P. Li et al., Phase transitions in the assembly of multivalent signalling proteins. Nature 483, 336-340 (2012).
6. Wei C, Jia L, Huang X, et al. CTCF organizes inter-A compartment interactions through RYBP-dependent phase separation. Cell Res. 2022;32(8):744-760.
7. Zhao C, Cai S, Shi R, et al. HERD-1 mediates multiphase condensate immiscibility to regulate small RNA-driven transgenerational epigenetic inheritance. Nat Cell Biol. 2024;26(11):1958-1970.
8. Soto JS, Jami-Alahmadi Y, Chacon J, et al. Astrocyte-neuron subproteomes and obsessive-compulsive disorder mechanisms. Nature. 2023;616(7958):764-773.
9. Ramelow CC, Dammer EB, Xiao H, et al. Simultaneous profiling of native-state proteomes and transcriptomes of neural cell types using proximity labeling. Preprint. bioRxiv. 2025;2025.01.29.635500. Published 2025 Feb 1.
