rPRO-seq全新首发,新生RNA测序新标杆!流程加速,更低样本量
rPRO-seq
新生RNA测序新标杆!流程加速,更低样本量
转录调控是基因表达的核心环节,传统RNA-seq技术往往只能检测稳态的RNA,而难以捕捉那些半衰期极短、不稳定或低丰度的转录本(如eRNA、lncRNA)。为了精准解析启动子近端RNA聚合酶II的暂停与释放、转录起始与延伸的精细调控,以及增强子转录活动等关键生物学过程,先后诞生了GRO-seq、SLAM-seq和PRO-seq等技术,经历一场从“稳态”到“动态”的深刻变革。其中PRO-seq可实现单碱基分辨率,但存在耗时耗力、样本需求高等局限。
rPRO-seq(Rapid Precision nuclear run-on sequencing)是PRO-seq的全新升级版本,在保持单碱基分辨率优势的同时,通过独特的接头设计和流程优化,极大地缩短了建库时间(~15 h),实现更低起始细胞量,解决了接头二聚体问题,显著提升建库效率和数据质量。适用于临床样本、稀有细胞类型。
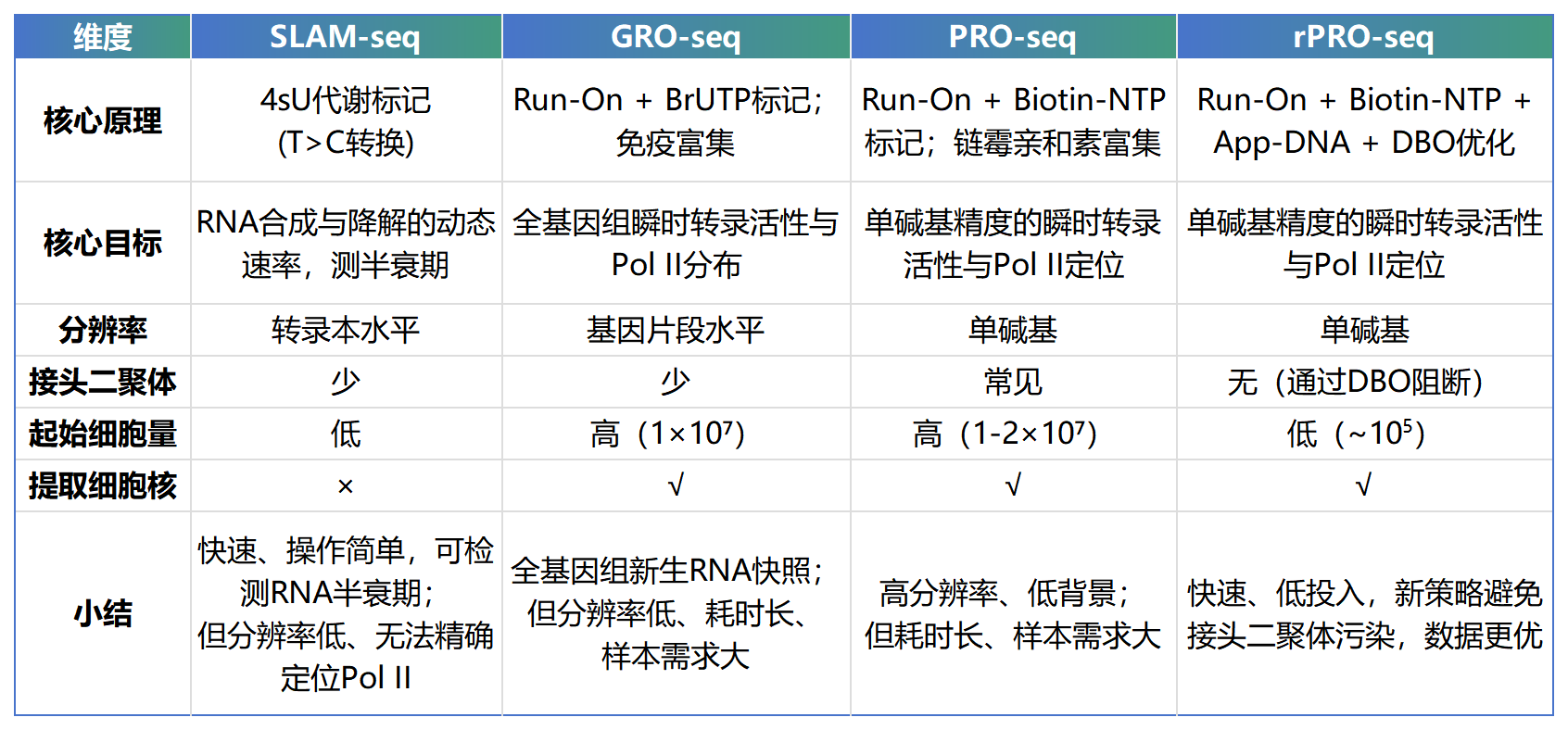
技术对比
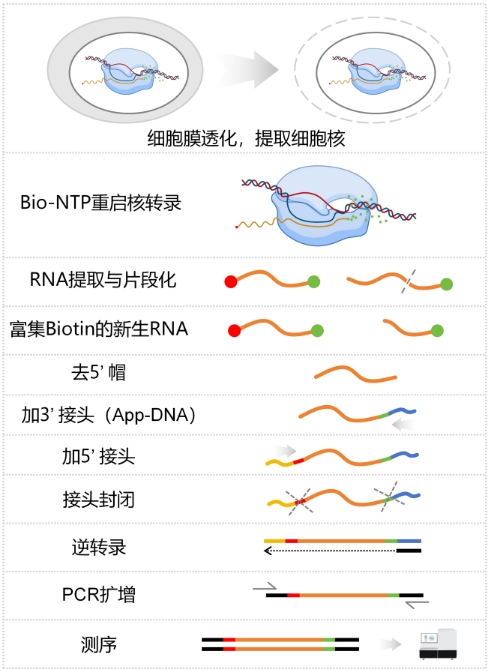
技术流程
为什么选择rPRO-seq?
📉实验周期大幅缩短
建库时间从4-5 d压缩至~15 h;加速项目周期,降低RNA降解风险;
📉起始细胞量大幅降低
最低仅需~10⁵个细胞(传统需1-2×10⁷),显著拓展了技术适用范围;
📈数据有效率大幅提升
App-DNA+DBO策略提高连接效率、避免接头二聚体生成,数据质量显著提升。
应用场景
1. 转录调控机制研究
(1)启动子近端暂停分析:单碱基精度定位RNA Pol II暂停位点,解析暂停释放调控机制;
(2)增强子功能研究:高灵敏度检测eRNA,绘制增强子-启动子调控网络。
2. 表观遗传调控研究
(1)染色质状态与转录偶联:结合ChIP-seq、CUT&Tag、ATAC-seq等数据,解析转录因子结合、组蛋白修饰或染色质开放程度与转录活性之间的关联;
(2)稳态RNA水平:对比新生RNA(生产速率)与稳态RNA(库存量),计算RNA的降解速率或合成效率,揭示转录后调控机制;
(3)三维基因组:联合HiChIP、Hi-C数据,将远端增强子(Enhancer)的转录信号与目标基因(Promoter)的转录信号通过物理接触关联起来,解析远距离调控机制;
(4)非编码RNA功能:检测上游反义转录、增强子RNA、长链非编码RNA等不稳定转录本。
3. 疾病机制与药物研发
(1)肿瘤转录依赖性评估:快速评估如BET抑制剂等表观药物的直接转录靶点;
(2)药物响应动力学:区分药物的直接转录效应与继发性适应反应;
(3)神经发育障碍研究:如研究揭示关键基因在神经元中调控神经发育相关基因的关键作用。
4. 发育与干细胞生物学
深入剖析胚胎干细胞、组织干细胞或稀有祖细胞(如造血祖细胞)在分化、自我更新过程中的瞬时转录重编程机制。
送样要求
仅限人、大小鼠,其他物种需评估
≥ 1×10^5
细胞
>85%
活率
分析内容
标准分析
1. 去接头、低质量reads
2. Reads基因组比对
3. 转录活跃区域识别
4. 启动子和基因体活性区域分类
5. 各区域read counts计算统计
6. Reads在转录起始位点(TSS)附近的meta分析;
7. Traveling Ratio分析:计算转录延伸效率(启动子/基因体信号比)
8. Traveling Matrix分析:二维分类转录状态变化(四象限分析)
9. 差异表达分析
10. GO/KEGG通路富集分析
高级分析
eRNA分析
个性化分析(评估收费)
Demo
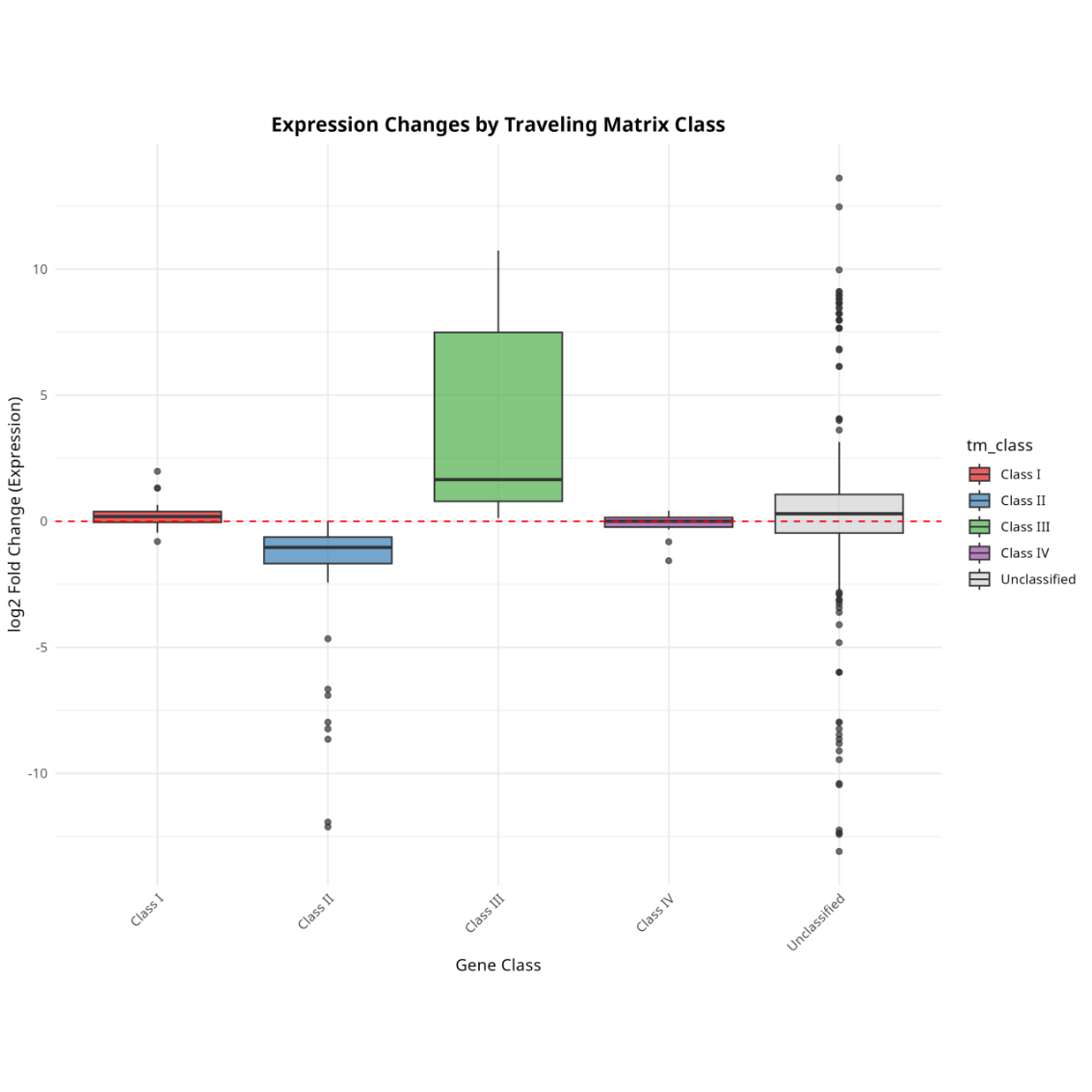
差异倍数在TM四类分布
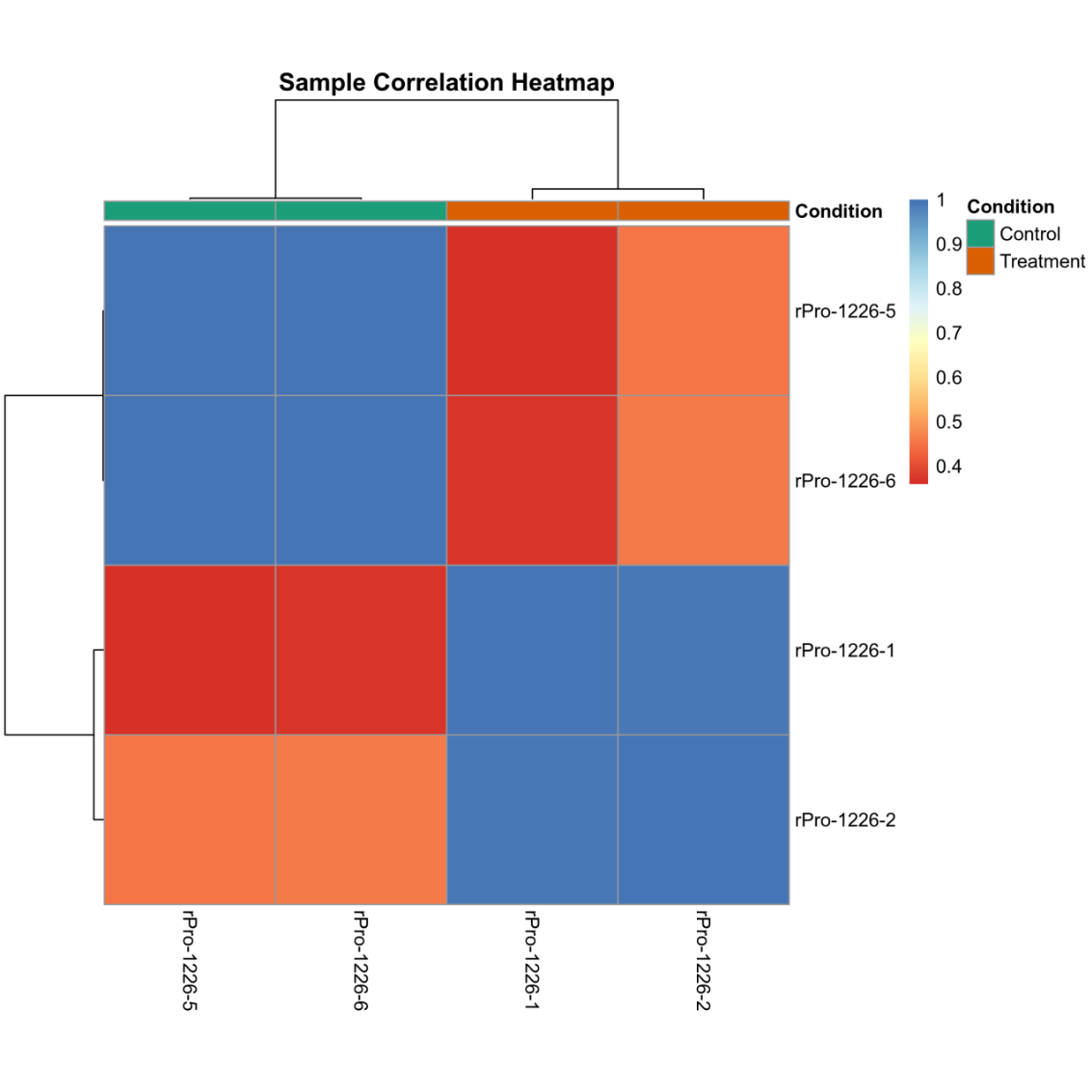
样本相关性图
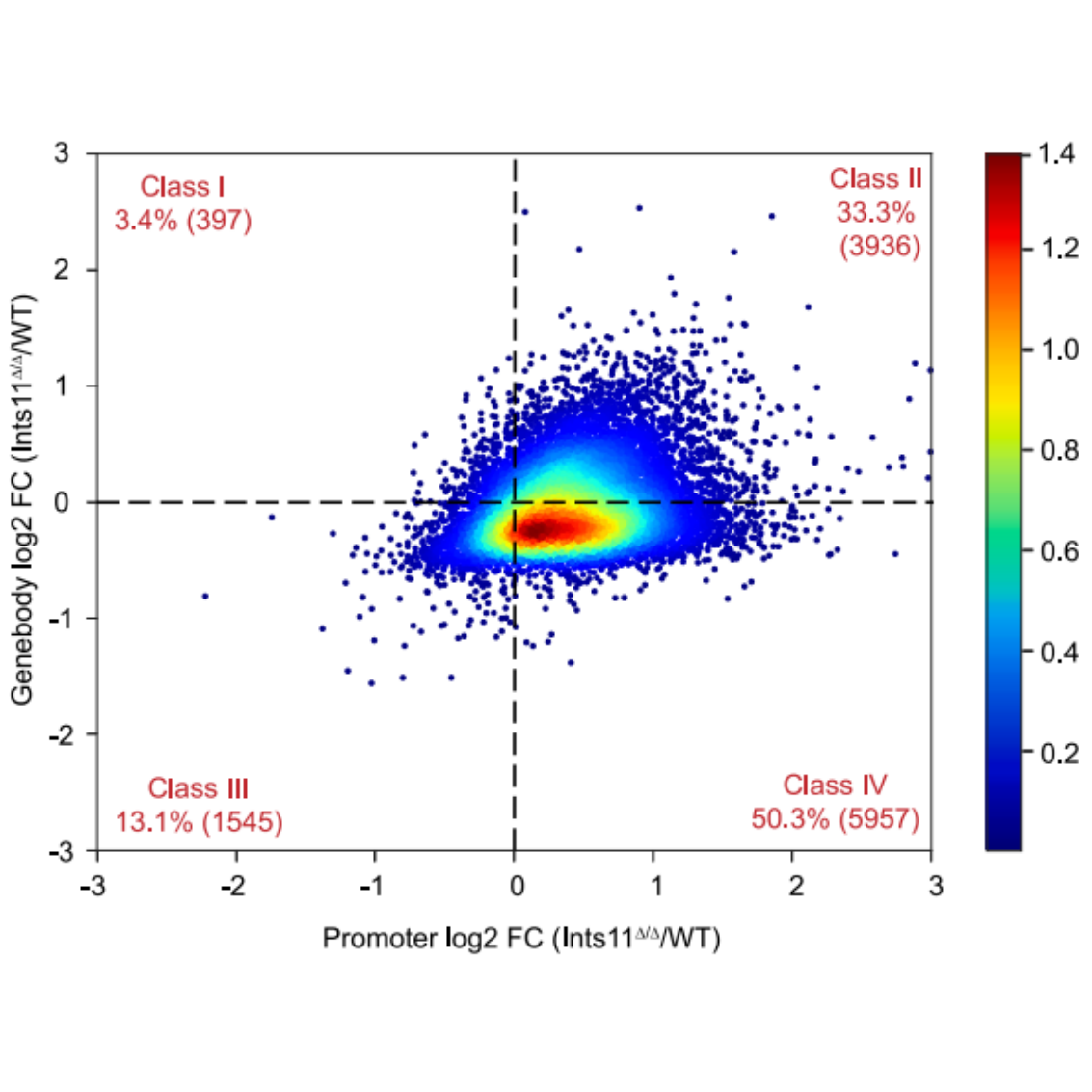
Traveling Matrix分类图(Cingaram PKR, et al. Mol Cell. 2025.)
注:
Class I: 转录暂停(启动子信号增加,基因体减少);Class II: 转录抑制(启动子和基因体信号都减少);Class III: 转录激活(启动子和基因体信号都增加);Class IV: 转录暂停释放(启动子信号减少,基因体增加)
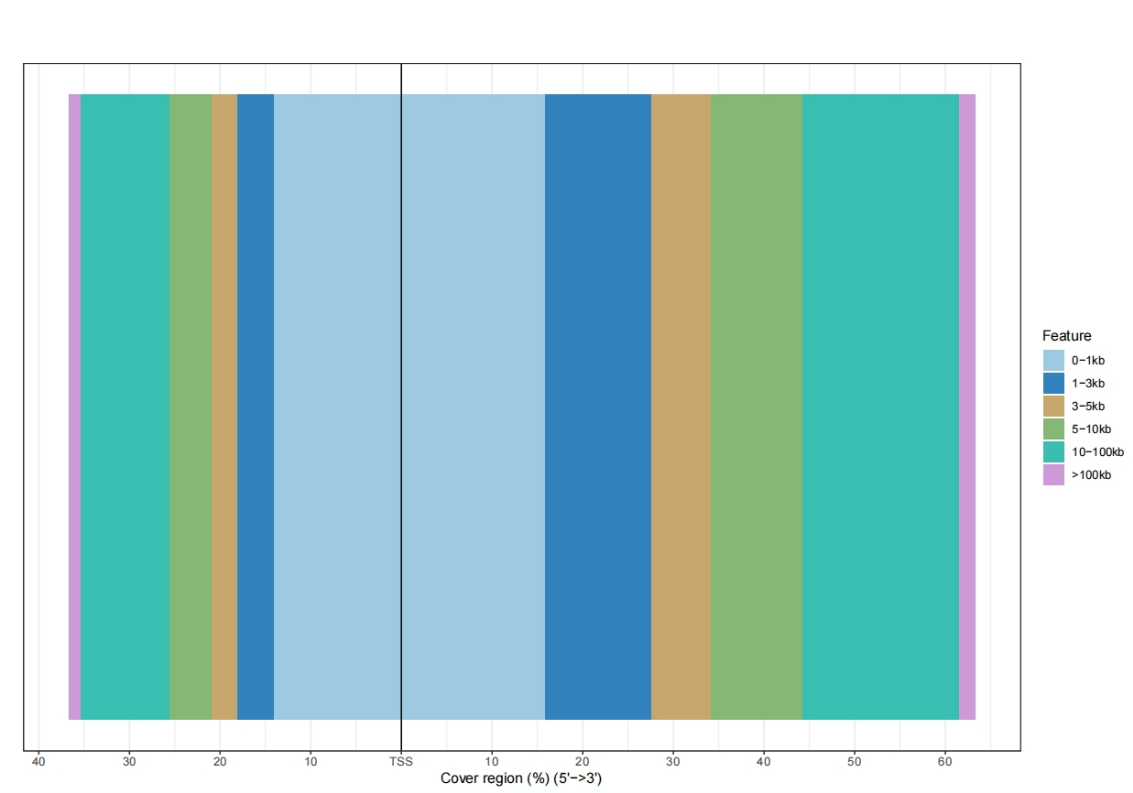
TSS距离分布图
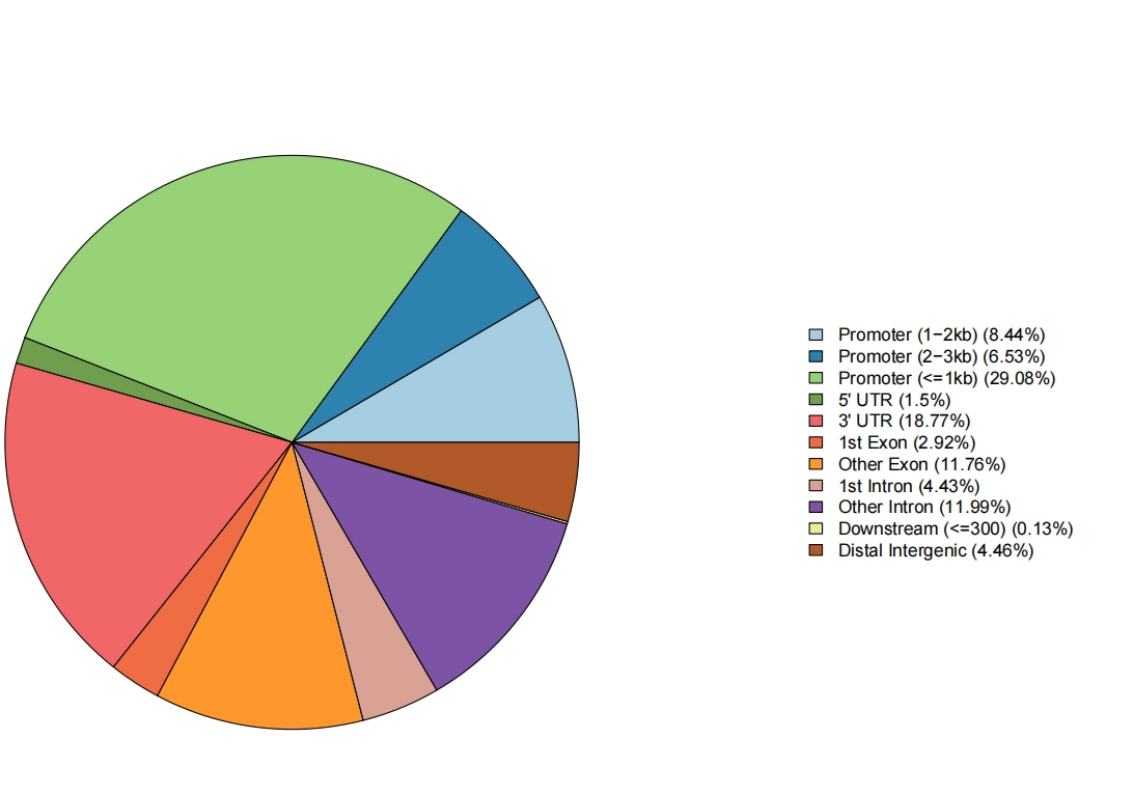
基因组区域注释饼图
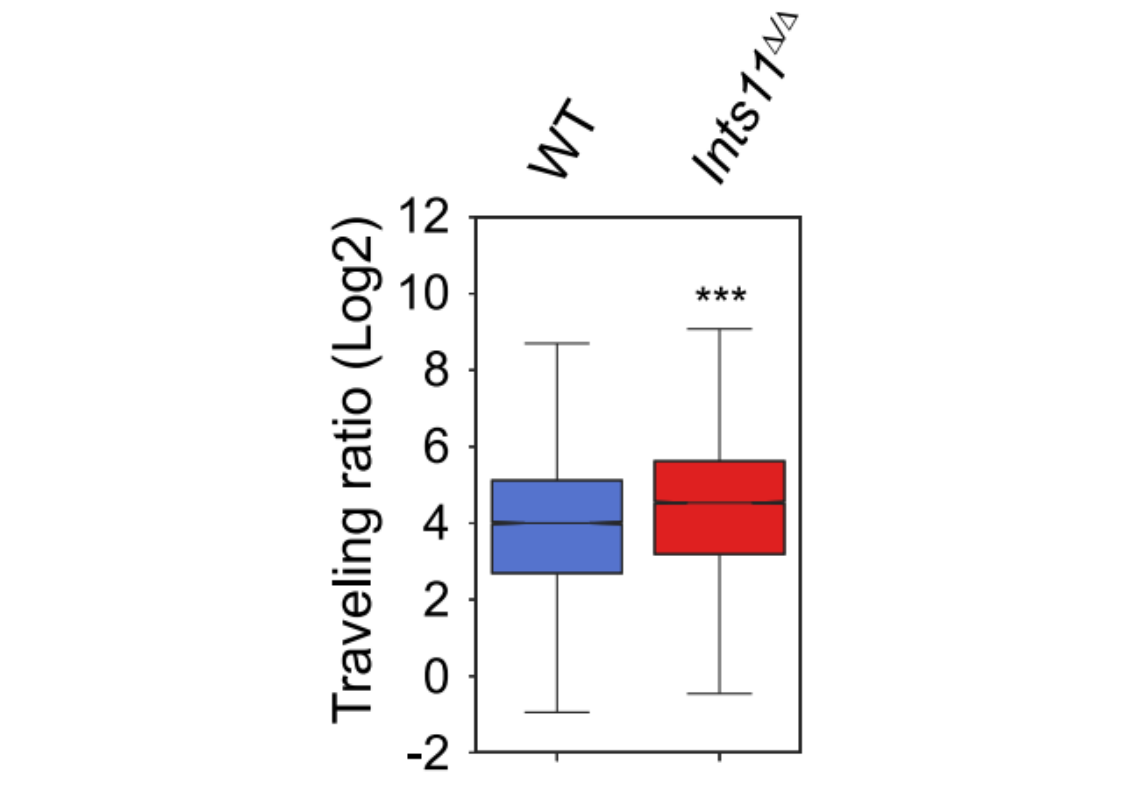
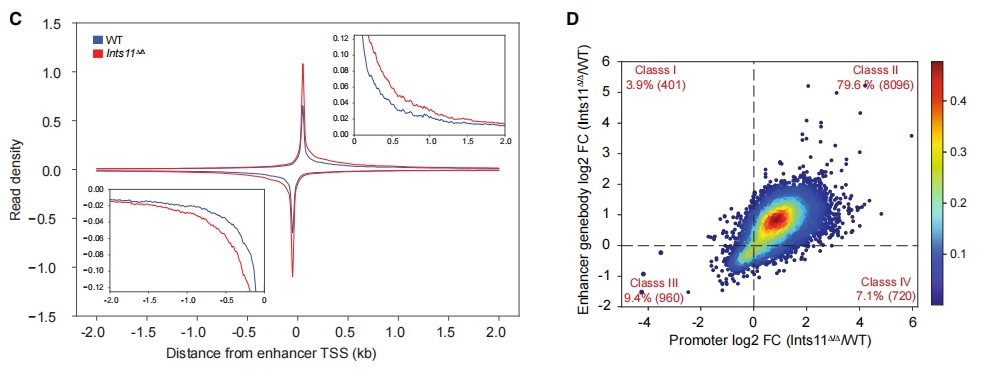
Traveling Ratio分析(Cingaram PKR, et al. Mol Cell. 2025.)

研究使用Ints11敲除小鼠模型,从50万个稀有造血祖细胞进行rPRO-seq分析。INTS11缺失导致3525个基因差异表达,下调基因富集于信号通路和mRNA加工。转录矩阵(TM)显示50%基因启动子聚合酶密度增加而基因体降低,反映暂停增强和延伸受损;90%增强子RNA转录延长,证实Integrator作为启动子近端终止复合物的功能。
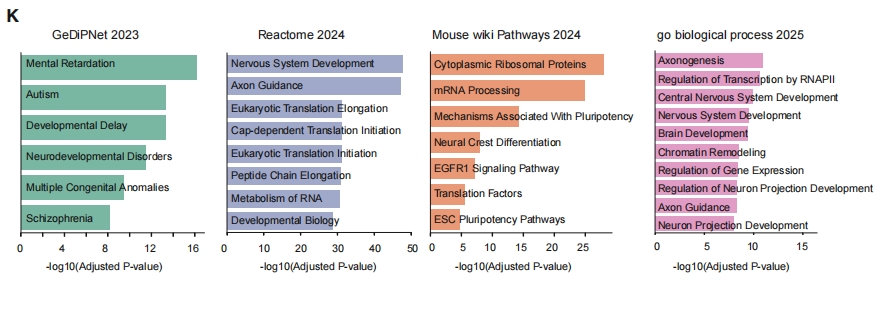
此外,将小鼠胚胎干细胞分化为神经元,通过INTS11-dTAG系统急性降解INTS11后进行rPRO-seq。结果显示神经元基因尤其是长基因(>20kb)出现聚合酶暂停和延伸缺陷。下调基因富集于神经发育障碍通路(神经元分化、突触组织、轴突发育等),直接靶基因包括自闭症风险基因SHANK3、突触相关基因NLGN/NRXN和谷氨酸受体GRIN2A/2B等,在转录层面阐明INTS11突变致病机制。
相关案例